Nome Comercial/ Apresentação
Purinethol (Mercaptopurina) 50mg / Comprimido
Classe Terapêutica
Agentes antineoplásicos, antimetabólitos, análogos da purina.
Indicação
Purinethol® é indicado para o tratamento de leucemia aguda. Pode ser utilizado na indução de remissão, sendo especialmente indicado para o tratamento de manutenção em leucemia linfoblástica aguda (LLA) e leucemia mieloide aguda (LMA).
Dose
Purinethol® deve ser administrado com alimentos ou com o estômago vazio, mas os pacientes devem padronizar o método de administração. A dose não deve ser administrada com leite ou produtos lácteos.
Purinethol® deve ser administrado pelo menos 1 hora antes ou 2 horas depois da ingestão de leite ou produtos lácteos.
Adultos e crianças: a dose usual é de 2,5 mg/kg ou 50 a 75 mg/m² de área de superfície corporal por dia. Porém, a dose e a duração da administração dependem da natureza e da posologia de outros agentes citotóxicos administrados conjuntamente com Purinethol®. A dose deve ser cuidadosamente ajustada para cada paciente individualmente.
Purinethol® tem sido usado em vários esquemas de tratamento combinado para leucemia aguda. A literatura deve ser consultada para obtenção de detalhes.
Estudos realizados em crianças com leucemia linfoblástica aguda sugerem que a administração de Purinethol® à noite diminui o risco de reincidência, em comparação com a administração pela manhã.
Idosos: é aconselhável o monitoramento das funções renal e hepática nesses pacientes, e se houver insuficiência, a redução da dose deve ser considerada.
Ajuste de dose
Insuficiência renal
Estudos com uma pró-droga da mercaptopurina não demonstraram nenhuma diferença na farmacocinética de mercaptopurina em pacientes urêmicos, em comparação com pacientes submetidos a transplante renal. Pouco se sabe sobre os metabólitos ativos da mercaptopurina na insuficiência renal. A mercaptopurina e/ou seus metabólitos são eliminados por hemodiálise, com aproximadamente 45% dos metabólitos radioativos eliminados durante a diálise de 8 horas.
Insuficiência hepática
Um estudo com uma pró-droga da mercaptopurina foi conduzido em três grupos de pacientes submetidos a transplante renal: aqueles sem doença hepática, aqueles com insuficiência hepática (mas sem cirrose) e aqueles com insuficiência hepática e cirrose. O estudo demonstrou que a exposição à mercaptopurina foi 1,6 vez mais alta em pacientes com insuficiência hepática (mas sem cirrose) e 6 vezes mais alta em pacientes com insuficiência hepática e cirrose, em comparação com os pacientes sem doença hepática.
Vias de administração
ORAL
Administração
Este comprimido não deve ser partido ou mastigado.
Cuidados específicos e monitoramento
O produto teve uma mudança em sua formulação em 14/04/2023 que pode afetar a velocidade de absorção, e que, portanto, o médico deve estar atento a possíveis sinais de toxicidade elevada ou de redução na duração do efeito do medicamento, para realizar os ajustes de dose que se fizerem necessários.
Purinethol® é um agente citotóxico ativo para uso sob a supervisão de médicos com experiência na administração desses agentes.
Imunização
A imunização com vacinas contendo microrganismos vivos tem o potencial de causar infecções em pacientes imunocomprometidos. Deste modo, não é recomendada a imunização com vacinas elaboradas com microrganismos vivos em pacientes diagnosticados com leucemia linfoblástica aguda e leucemia mieloide aguda. Em todos os casos, os pacientes em remissão não devem receber vacinas contendo microrganismos vivos até que o paciente seja considerado apto a responder à vacina. O intervalo entre a descontinuação da quimioterapia e a restauração da capacidade do paciente de responder à vacina depende da intensidade e do tipo de medicamentos causadores de imunossupressão utilizados, da doença subjacente e de outros fatores.
Ribavirina
A coadministração de ribavirina e Purinethol® não é aconselhável. A ribavirina pode reduzir a eficácia e aumentar a toxicidade da mercaptopurina.
Monitoramento
Como o Purinethol® é altamente mielossupressor, recomenda-se a realização de contagens sanguíneas totais diariamente, durante a indução da remissão. Os pacientes devem ser cuidadosamente monitorados durante o tratamento.
Supressão da medula óssea
O tratamento com mercaptopurina causa supressão da medula óssea, a qual leva à leucopenia, à trombocitopenia e, com menor frequência, à anemia. Durante a indução da remissão, deve ser realizada frequentemente a contagem sanguínea completa. Durante a terapia de manutenção, deve ser realizado regularmente monitoramento cuidadoso dos parâmetros hematológicos e mais frequentemente se doses altas são utilizadas ou caso haja disfunção hepática e/ ou renal severa.
Um aumento no monitoramento hematológico do paciente é aconselhado caso diferentes formulações farmacêuticas de mercaptopurina sejam alternadas.
As contagens de leucócitos e plaquetas continuam a cair após a suspensão do tratamento, de modo que, ao primeiro sinal de uma queda muito grande nessas contagens, o tratamento deve ser interrompido imediatamente. A supressão da medula óssea é reversível, se Purinethol® for suspenso com suficiente antecedência.
Durante a indução de remissão na leucemia mieloide aguda, o paciente pode, frequentemente, ter que passar por um período de relativa aplasia da medula óssea, sendo importante a disponibilidade de condições de suporte adequadas.
A dose de mercaptopurina pode precisar ser reduzida quando este agente for combinado com outras drogas cuja toxicidade primária ou secundária é mielossupressão.
Hepatotoxicidade
Purinethol® é hepatotóxico, sendo assim, testes de função hepática devem ser feitos semanalmente durante o tratamento. Os níveis de gama glutamil transferase (GGT) no plasma podem ser particularmente preditivos de abstinência devido à hepatotoxicidade. É aconselhável um controle mais frequente em pacientes com doença hepática pré-existente ou que foram tratados com outra droga potencialmente hepatotóxica. Se aparecer icterícia, o paciente deve ser instruído a descontinuar o tratamento com Purinethol® imediatamente.
Síndrome de lise tumoral
Durante a indução da remissão, quando estiver ocorrendo rápida lise celular, os níveis de ácido úrico no sangue e na urina devem ser controlados, pois pode haver desenvolvimento de hiperuricemia e/ou hiperuricosúria, com o risco de nefropatia por ácido úrico.
Deficiência da TPMT
Pacientes portadores de deficiência hereditária da enzima tiopurina S-metiltransferase (TPMT) podem apresentar sensibilidade não usual ao efeito mielossupressivo da mercaptopurina e podem ser suscetíveis a desenvolver supressão da medula óssea após o início do tratamento com Purinethol®.
É possível que esse problema seja exacerbado pela coadministração com medicamentos que inibem TPMT, como olsalazina, mesalazina ou sulfasalazina. Em indivíduos que recebem concomitantemente mercaptopurina e outros agentes citotóxicos, tem sido relatado uma possível associação da diminuição da atividade da TPMT e o desenvolvimento de mielodisplasia e leucemias secundárias.
Aproximadamente 0,3% (1:300) dos pacientes têm pouca ou nenhuma atividade enzimática detectável. Aproximadamente 10% dos pacientes têm atividade TPMT baixa ou intermediária e quase 90% dos indivíduos têm atividade TPMT normal. Também pode haver um grupo de aproximadamente 2% que tenha uma atividade TPMT muito alta.
Alguns laboratórios realizam testes para detectar a deficiência da TPMT. Entretanto, esses testes não conseguem identificar todos os pacientes com risco de toxicidade severa. Portanto, é necessário fazer um rigoroso monitoramento dos hemogramas do paciente.
Mutação no gene NUDT15
Pacientes com o gene NUDT15 mutado herdado têm um risco aumentado de toxicidade severa por tiopurina, como leucopenia e alopecia precoces, de doses convencionais de terapia com tiopurina e geralmente requerem substancial redução da dose. Pacientes de etnia asiática estão particularmente sob risco, devido ao aumento da frequência da mutação nessa população. A dose inicial ideal para pacientes com deficiência heterozigótica ou homozigótica não foi estabelecida.
O teste genotípico e fenotípico das variantes do NUDT15 deve ser considerado antes de iniciar a terapia com tiopurina em todos os pacientes (incluindo pacientes pediátricos) para reduzir o risco de leucocitopenia severa relacionada à tiopurina e alopecia, especialmente em populações asiáticas.
Resistência cruzada
Tem-se observado uma resistência cruzada entre a mercaptopurina e 6-tioguanina.
Hipersensibilidade
Os pacientes com suspeita de reação prévia à hipersensibilidade a mercaptopurina não devem ter como recomendação o uso de sua pró-droga azatioprina, a menos que o paciente tenha sido confirmado como hipersensível à mercaptopurina com testes alergológicos e tenha sido negativo para azatioprina. Como a azatioprina é uma pró-droga da mercaptopurina, deve-se avaliar os pacientes com história prévia de hipersensibilidade à azatioprina quanto à hipersensibilidade a 6- mercaptopurina antes do início do tratamento.
Insuficiência renal e/ou hepática
Recomenda-se cautela durante a administração de Purinethol® em pacientes com insuficiência renal e/ou hepática. Deve-se cogitar reduzir a dose nesses pacientes, devendo a resposta hematológica ser cuidadosamente monitorada.
Mutagenicidade e carcinogenicidade
Os pacientes que recebem terapia imunossupressora, incluindo mercaptopurina, têm um risco aumentado de desenvolver distúrbios linfoproliferativos e outras malignidades, notadamente cânceres de pele (melanoma e não-melanoma), sarcomas (de Kaposi e não-Kaposi) e câncer cervical uterino in situ. O aumento do risco parece estar relacionado ao grau e duração da imunossupressão. Tem sido relatado que a descontinuação da imunossupressão pode fornecer regressão parcial do distúrbio linfoproliferativo.
Um regime de tratamento contendo vários imunossupressores (incluindo tiopurinas) deve, portanto, ser usado com cautela, pois isso poderia levar a distúrbios linfoproliferativos, alguns com fatalidades relatadas. Uma combinação de múltiplos imunossupressores, administrada concomitantemente, aumenta o risco de distúrbios linfoproliferativos associados ao vírus de Epstein-Barr (EBV).
Aumento do número de aberrações cromossômicas foi observado nos linfócitos periféricos em pacientes leucêmicos, em um paciente com hipernefroma (o qual recebeu uma dose não declarada da mercaptopurina) e em pacientes com nefropatia crônica tratados com doses de 0,4 – 1,0 mg/kg/dia.
Dois casos foram documentados sobre a ocorrência de leucemia não-linfática aguda em pacientes tratados com mercaptopurina em associação com outras drogas para distúrbios não-neoplásicos.
Um caso isolado foi relatado em que um paciente, em tratamento para pioderma gangrenoso com mercaptopurina, desenvolveu, posteriormente, leucemia aguda não-linfática. Porém, não ficou estabelecido se existe uma relação causal com a droga ou se o fato estava diretamente relacionado com o histórico natural da doença.
Um paciente com doença de Hodgkin, tratado com mercaptopurina e agentes citotóxicos adicionais, desenvolveu leucemia mieloide aguda.
Doze anos e meio após tratamento com mercaptopurina para miastenia grave, uma paciente do sexo feminino desenvolveu leucemia mieloide crônica.
Foram recebidos relatos de linfoma hepatoesplênico de células T ocorrido em pacientes com Doença Inflamatória Intestinal (DII) – Doença de Crohn e Colite Ulcerativa, quando Purinethol® foi usado em combinação com agentes anti- TNF.
Síndrome de ativação macrofágica
A síndrome de ativação macrofágica (SAM) é um distúrbio conhecido que ameaça a vida e pode se desenvolver em pacientes com doenças autoimunes, em particular com doença inflamatória intestinal (DII), e poderia haver uma maior suscetibilidade ao desenvolvimento da doença com o uso de mercaptopurina. Se a SAM ocorrer ou houver suspeita, a avaliação e o tratamento devem ser iniciados o mais cedo possível, e o tratamento com mercaptopurina deve ser descontinuado. Os médicos devem estar atentos aos sintomas de infecção, como o EBV e o citomegalovírus (CMV), pois são gatilhos conhecidos para a SAM.
Distúrbios metabólicos e nutricionais
A administração de análogos de purina (azatioprina e mercaptopurina) pode interferir na via da niacina, levando potencialmente à deficiência de ácido nicotínico/Pelagra. Poucos casos foram relatados com o uso de azatioprina, especialmente em pacientes com DII – Doença de Crohn e Colite Ulcerativa. O diagnóstico de Pelagra deve ser considerado em um paciente que apresenta erupção cutânea pigmentada localizada (dermatite); gastroenterite (diarreia); e déficits neurológicos generalizados, incluindo declínio cognitivo (demência). A redução da dose ou a descontinuação do tratamento com mercaptopurina pode não ser necessária se for iniciado tratamento médico apropriado com suplementação de niacina/nicotinamida. No entanto, é necessária uma avaliação cuidadosa do risco-benefício caso a caso.
População pediátrica
Foram notificados casos de hipoglicemia sintomática em crianças com LLA recebendo mercaptopurina. A maioria dos casos notificados foi em crianças com menos de seis anos ou com um baixo índice de massa corporal.
Colestase da Gravidez
Colestase da gravidez tem sido ocasionalmente relatada em associação à terapia com mercaptopurina. O monitoramento da 6-metil mercaptopurina (6-MMP) deve ser considerado na presença de prurido com níveis elevados de ácidos biliares séricos totais maternos no segundo trimestre de gravidez, para estabelecer um diagnóstico precoce e minimizar o impacto no feto. Se ocorrer colestase da gravidez, é necessária uma avaliação caso a caso, considerando o perfil de risco-benefício do produto (potencial retirada/redução da dose).
Infecções
Pacientes tratados com mercaptopurina em monoterapia, ou em combinação com outros agentes imunossupressores, incluindo corticosteroides, mostraram maior suscetibilidade a infecções virais, fúngicas e bacterianas, incluindo infecção severa ou atípica, e reativação viral. A doença infecciosa e as complicações podem ser mais severas nesses pacientes do que em pacientes não tratados.
A exposição prévia ao vírus ou a infecção com o vírus da varicela zoster deve ser verificada antes do início do tratamento. Diretrizes locais podem ser consideradas, incluindo terapia profilática, se necessário. O teste sorológico antes do início do tratamento deve ser considerado em relação à hepatite B. Diretrizes locais podem ser consideradas, incluindo terapia profilática para casos que tenham testes sorológicos com resultado positivo. Se o paciente estiver infectado durante o tratamento, medidas apropriadas devem ser tomadas, que podem incluir terapia antiviral e cuidados de suporte.
Síndrome de Lesch-Nyhan
Evidências limitadas sugerem que nem a mercaptopurina nem a sua pró-droga, azatioprina, são eficazes em pacientes com a doença hereditária rara de deficiência completa de hipoxantinaguanina-fosforribosiltransferase (síndrome de Lesch-Nyhan). O uso de mercaptopurina ou azatioprina não é recomendado nesses pacientes.
Exposição UV
Os pacientes tratados com mercaptopurina são mais sensíveis ao sol. A exposição à luz solar e à luz ultravioleta deve ser limitada, e os pacientes devem ser recomendados a usar roupas de proteção e usar protetor solar com alto fator de proteção.
Inibidores da xantina oxidase
Os pacientes tratados com os inibidores da xantina oxidase alopurinol, oxipurinol ou tiopurinol, e mercaptopurina devem receber apenas 25% da dose habitual de mercaptopurina, uma vez que o alopurinol diminui a taxa de catabolismo da mercaptopurina.
Anticoagulantes
A inibição do efeito anticoagulante da varfarina e do acenocumarol foi notificada quando coadministrados com mercaptopurina. Deste modo, podem ser necessárias doses mais elevadas do anticoagulante.
Efeitos na capacidade de dirigir veículos e operar máquinas
Não existem dados sobre o efeito de Purinethol® na capacidade de dirigir e operar máquinas. Nenhum efeito prejudicial nessas atividades pode ser previsto a partir da farmacologia da droga.
Uso em idosos
Nenhum estudo específico foi conduzido em idosos. No entanto, é aconselhável monitorar as funções renal e hepática nesses pacientes e, se houver alguma insuficiência, deve-se considerar a redução da dose de Purinethol®.
Gravidez
Observou-se a ocorrência de substancial passagem transplacentária e transamniótica da mercaptopurina e seus metabólitos da mãe para o feto. O uso de mercaptopurina deve ser evitado sempre que possível durante a gravidez, particularmente durante o primeiro trimestre. Em qualquer caso individual, o risco potencial para o feto deve ser equilibrado com o benefício esperado para a mãe.
Como em toda quimioterapia citotóxica, devem ser tomadas medidas contraceptivas em caso de algum dos parceiros estar em tratamento com Purinethol® e por até 3 meses após a última dose do medicamento.
Estudos de mercaptopurina em animais mostraram toxicidade reprodutiva. O risco potencial para os seres humanos é em grande parte desconhecido.
Colestase da gravidez foi ocasionalmente relatada em associação com terapia com mercaptopurina. O diagnóstico precoce e a descontinuação da mercaptopurina podem minimizar o impacto ao feto. No entanto, uma avaliação cuidadosa do benefício para a mãe e do impacto sobre o feto deve ser realizada, se colestase da gravidez é confirmada.
Exposição materna: Tem-se observado o nascimento de bebês normais após a administração de Purinethol®, como único agente quimioterápico, durante a gravidez, particularmente antes da concepção e após o primeiro trimestre. Abortamentos e nascimentos prematuros foram relatados em mulheres expostas durante a gestação. Diversos casos de nascimentos de bebês com anormalidades congênitas múltiplas foram relatados em mulheres que receberam tratamento com Purinethol® em combinação com outros agentes citotóxicos.
Exposição paterna: Tem-se observado anormalidades congênitas e abortos espontâneos posteriores a exposição paterna ao Purinethol®.
Lactação
A mercaptopurina tem sido detectada no leite materno em pacientes que sofreram transplante renal e recebendo terapia imunossupressora com um pró-fármaco da mercaptopurina. Recomenda-se que mulheres fazendo uso de Purinethol® não devam amamentar.
Fertilidade
O efeito da terapia com mercaptopurina na fertilidade humana é desconhecido. Há relatos de paternidade/maternidade bem sucedida após receber tratamento durante a infância ou adolescência. A oligospermia transitória foi relatada após exposição à mercaptopurina.
Categoria D de risco da gravidez: Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez.
Medicamentos imunossupressores podem ativar focos primários de tuberculose. Os médicos que acompanham pacientes sob imunossupressão devem estar atentos quanto à possibilidade de surgimento de doença ativa, tomando, assim, todos os cuidados para o diagnóstico precoce e o tratamento.
Interações medicamentosas
Em indivíduos imunocomprometidos, não é recomendada a utilização de vacinas com microrganismos vivos.
Efeito de fármacos concomitantes sobre Purinethol®
Ribavirina
A ribavirina inibe a enzima inosina monofosfato desidrogenase (IMPDH), levando a uma menor produção de nucleotídeos 6-tioguanina ativos. Mielossupressão severa foi relatada após a administração concomitante de uma pró-droga da mercaptopurina e ribavirina. Portanto, a administração concomitante de ribavirina e Purinethol® não é aconselhável.
Agentes mielossupressores
Quando Purinethol® é combinado com outros agentes mielossupressores, é preciso ter cautela. Reduções da dose podem ser necessárias, com base no monitoramento hematológico.
Alopurinol / oxipurinol / tiopurinol ou outros inibidores de xantina oxidase
A atividade de xantina oxidase é inibida pelo alopurinol, oxipurinol e tiopurinol, o que resulta em conversão reduzida de ácido 6-tioinosínico biologicamente ativo para ácido 6-tioúrico biologicamente inativo. Quando alopurinol, oxipurinol e/ou tiopurinol e a mercaptopurina são administrados concomitantemente, é essencial que seja administrada apenas 25% da dose usual da mercaptopurina.
Outros inibidores da xantina oxidase, como o febuxostate, podem diminuir o metabolismo da mercaptopurina. A administração concomitante não é recomendada, uma vez que os dados são insuficientes para determinar uma redução adequada da dose.
Aminossalicilatos
Existem evidências in vitro e in vivo de que os derivados de aminossalicilatos (como olsalazina, mesalazina e sulfassalazina) inibem a enzima TPMT. Portanto, pode ser necessário considerar a administração de doses mais baixas de Purinethol® quando o fármaco for administrado concomitantemente com derivados de aminossalicilato.
Metotrexato
O metotrexato, na dose 20 mg/m², por via oral, aumentou a AUC da mercaptopurina em aproximadamente 31%, e, na dose de 2 ou 5 g/m², por via intravenosa, aumentou a AUC da mercaptopurina em 69% e 93%, respectivamente. Portanto, quando a mercaptopurina for administrada concomitantemente com metotrexato em dose alta, a dose deve ser ajustada, para manter-se uma contagem de leucócitos adequada.
Infliximabe
Interações têm sido observadas entre a azatioprina, pró-droga da mercaptopurina e o infliximabe. Os pacientes que receberam azatioprina em curso experimentaram aumentos transitórios nos níveis de 6-TGN (nucleotídeo de 6-tioguanina, um metabólito ativo da azatioprina) e diminuições na contagem média de leucócitos nas primeiras semanas após a infusão de infliximabe, que retornou aos níveis anteriores após três meses.
Efeito de Purinethol® sobre outros fármacos
Anticoagulantes
A inibição do efeito anticoagulante de varfarina e acenocumarol foi relatada quando esses fármacos foram coadministrados com Purinethol®. Portanto, doses mais altas de anticoagulantes podem ser necessárias. Recomenda-se que os testes de coagulação sejam rigorosamente monitorados quando anticoagulantes forem administrados concomitantemente com Purinethol®.
Outras interações
A administração de mercaptopurina com alimentos pode diminuir ligeiramente a exposição sistêmica. A mercaptopurina pode ser administrada com alimentos ou com o estômago vazio, mas os pacientes devem padronizar o método de administração para evitar uma grande variabilidade na exposição.
A dose não deve ser administrada com leite ou produtos lácteos, uma vez que esses alimentos contêm xantina oxidase, uma enzima que metaboliza a mercaptopurina e pode, portanto, conduzir a concentrações plasmáticas reduzidas de mercaptopurina.
Estabilidade/ Conservação
O medicamento deve ser mantido em sua embalagem original. Armazenar em temperatura ambiente (de 15°C a 30 °C). Proteger da luz e da umidade.
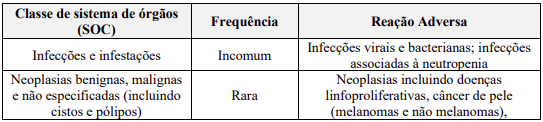
Reações adversas
Resumo do perfil de segurança
Não há documentação clínica atualizada sobre o efeito de Purinethol® que possam servir de base para determinar precisamente a frequência da ocorrência de efeitos adversos. As categorias de frequência atribuídas às reações adversas a medicamentos abaixo são estimativas: para a maioria das reações, dados adequados para o cálculo da incidência não estão disponíveis. Os efeitos adversos podem variar na sua incidência dependendo da dose recebida e, também quando administrados em combinação com outros agentes terapêuticos.
O principal efeito colateral do tratamento com mercaptopurina é a supressão da medula óssea, levando a leucopenia e trombocitopenia.
Resumo tabelado das reações adversas
A convenção a seguir tem sido utilizada para a classificação de frequência:
Muito comum (> 1/10)
Comum (> 1/100 e ≤ 1/10)
Incomum (> 1/1.000 e ≤ 1/100)
Rara (> 1/10.000 e ≤ 1/1.000)
Muito rara (≤ 1/10.000)
Desconhecida (não pode ser estimada a partir dos dados disponíveis)
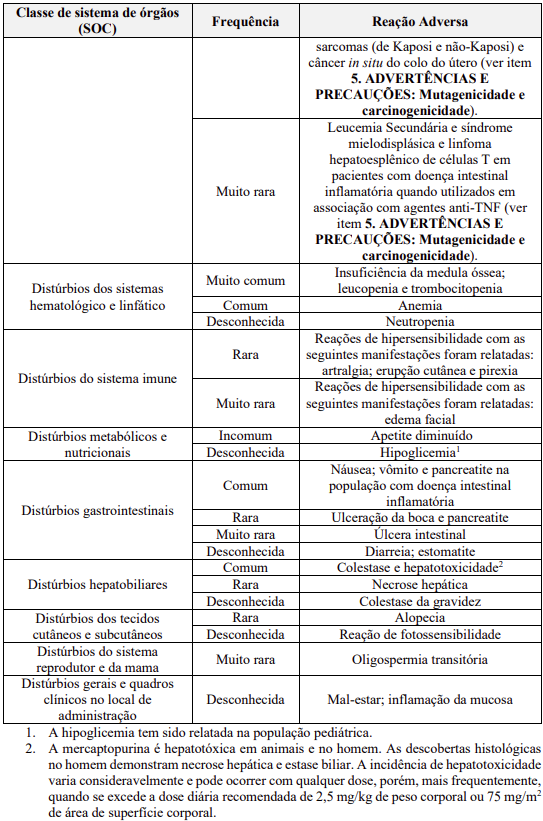
O controle da função hepática, através de testes, pode permitir detecção antecipada da hepatotoxicidade. Os níveis de gama glutamil transferase (GGT) no plasma podem ser particularmente preditivos de abstinência devido à hepatotoxicidade. A hepatotoxicidade é normalmente reversível caso o tratamento com a mercaptopurina seja interrompido a tempo de evitar a falência hepática fatal.
Contraindicações
O uso de Purinethol® é contraindicado para pacientes com hipersensibilidade conhecida a qualquer componente da fórmula. Tendo-se em vista a gravidade das indicações, não existe nenhuma contraindicação absoluta ao uso de Purinethol®.
Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez. Atenção: Contém lactose. Este medicamento não deve ser usado por pessoas com síndrome de má-absorção de glicose-galactose.
Fonte:
Purinethol®. [Bula]. São Paulo: Aspen Pharma Indústria Farmacêutica Ltda. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=137640133: 14/08/2025
