Nome Comercial e Princípio Ativo / Apresentação:
XELODA
capecitabina 150 mg comprimido revestido.
capecitabina 500 mg comprimido revestido.
Classe Terapêutica:
Antineoplásico, análogo de fluoropirimidina
Indicação:
Câncer de mama metastático: em monoterapia (resistência a antraciclina e taxano) ou em combinação com docetaxel.
Câncer colorretal: tratamento adjuvante em pacientes com câncer colorretal Dukes C (estágio 3), primeira e segunda linha em doença metastática (isolada ou em combinação com oxaliplatina/bevacizumabe).
Câncer gástrico avançado: primeira linha em combinação com derivados de platina (cisplatina ou oxaliplatina).
Dose:
Monoterapia:
Recomendado 1.250 mg/m² – 2x/dia, por 14 dias, seguido de 7 dias de descanso.
Terapia combinada:
– Câncer de mama: Em combinação com docetaxel, a dose recomendada de Capecitabina é de 1.250 mg/m2, duas vezes ao dia (pela manhã e à noite; equivalente a dose total diária de 2.500 mg/m2) durante 14 dias, seguidos de sete dias de descanso, associado ao docetaxel, 75 mg/m2, por infusão intravenosa durante uma hora, a cada três semanas
– Câncer colorretal e gástrico: A dose inicial recomendada de Capecitabina é de 800 a 1.000 mg/m2 administrada duas vezes ao dia durante duas semanas, seguida de um período de sete dias de descanso, ou 625 mg/m2 duas vezes ao dia quando administrada continuamente.
As tabelas a seguir mostram exemplos de cálculos da dose recomendada e da dose reduzida para uma dose inicial de 1.250 mg/m2 ou 1.000 mg/m2.
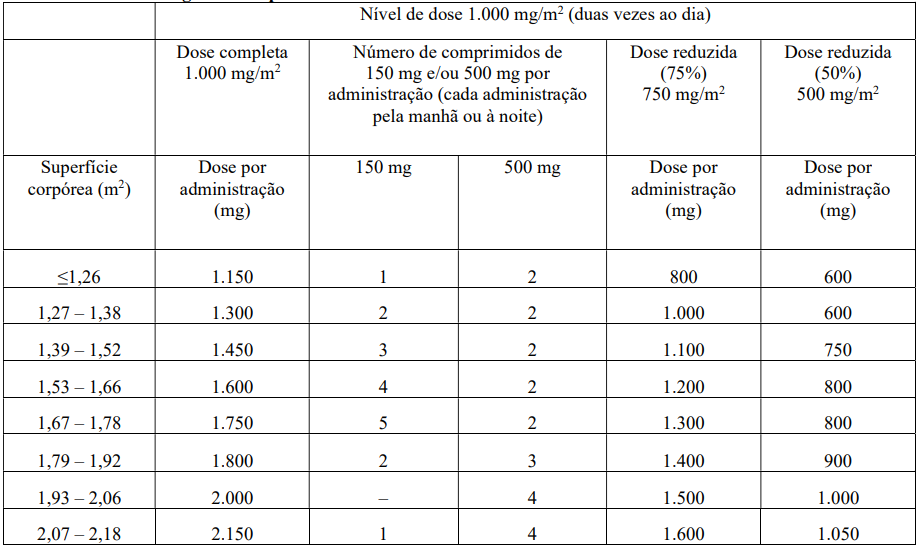
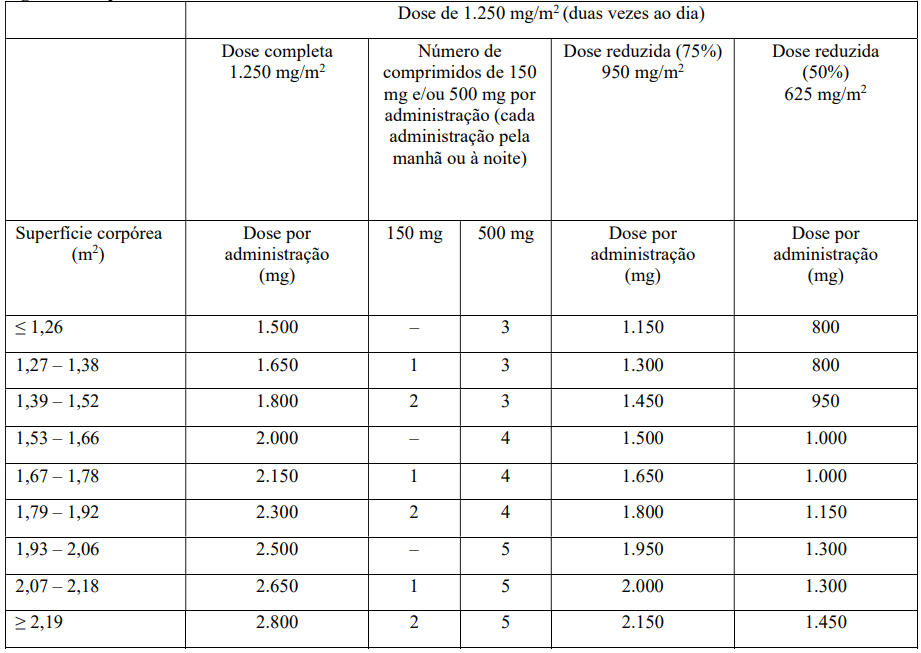
Dose Máxima:
Definida de acordo com a superfície corporal, não ultrapassar o regime descrito em bula (1.250 mg/m² 2x/dia).
Ajuste de dose:
Paciente pediátrico:
A segurança e a eficácia de capecitabina em pacientes pediátricos ainda não foram estabelecidas.
Paciente geriátrico:
Em tratamento combinado de Capecitabia mais Docetaxel, recomenda-se a redução da dose inicial de capecitabina para 75% (950 mg/m2 duas vezes ao dia).
Insuficiência renal:
[depuração de creatinina 51 – 80 mL/min (Cockroft e Gault)]: Não se recomendam ajustes da dose inicial.
[depuração de creatinina 30 – 50 mL/min (Cockroft e Gault)]: Reduzir a dose para 75%, para uma dose inicial de 950 mg/m2.
[depuração de creatinina < 30 mL/min (Cockroft e Gault)]: Capecitabina deve ser descontinuado.
Insuficiência hepática:
Em pacientes com disfunção hepática leve a moderada nenhum ajuste da dose inicial é necessário.
Vias de administração:
VIA ORAL
Administração:
Administrar até 30 minutos após a refeição.
Cuidados e orientações:
Pacientes com disfunção hepática, devem ser cuidadosamente monitorados.
Este medicamento não deve ser partido, aberto ou mastigado.
Interações Medicamentosas:
Uso de Sorivudina durante o tratamento com Capecitabina interagem aumentando a toxicidade das fluoropirimidinas, que é potencialmente fatal
Estabilidade/ Conservação:
Conservar em temperatura ambiente (15–30 ºC).
Manter na embalagem original, protegido da umidade.
Contraindicações:
Capecitabina está contraindicado a pacientes com hipersensibilidade conhecida à capecitabina ou a quaisquer excipientes da fórmula do produto.
Capecitabina está contraindicado a pacientes que apresentam história de reações graves e inesperadas à terapia com fluoropirimidinas ou com hipersensibilidade conhecida à fluoruracila.
Capecitabina não deve ser administrado concomitantemente com sorivudina ou com seus análogos quimicamente relacionados, como a brivudina.
Categoria de risco na gravidez: D. Este medicamento não deve ser utilizado por mulheres grávidas
Reações adversas:
Muito comuns: diarreia, náusea, vômito, estomatite, dor abdominal, fadiga, alopecia, eritema palmo-plantar, anorexia.
Comuns: neutropenia, trombocitopenia, febre, desidratação, rash cutâneo.
Raras: insuficiência hepática, síndrome coronariana aguda, arritmias, reações cutâneas graves.
Fonte:
XELODA®. [Bula]. São Paulo: LABORATÓRIO QUÍMICO FARMACÊUTICO BERGAMO LTDA. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=106460222: 01/06/2023
XELODA®. [Bula]. São Paulo: EUROFARMA LABORATÓRIOS S.A. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=100431209: 09/08/2022
