VECTIBIX® (panitumumabe) Solução para Diluição para Infusão com 20 mg/mL em frasco-ampolas de 5 mL.
Nome Comercial e Princípio Ativo / Apresentação:
VECTIBIX® (panitumumabe) Solução para Diluição para Infusão com 20 mg/mL em frasco-ampolas de 5 mL.
Classe Terapêutica: Antineoplásicos, anticorpos monoclonais.
Indicação:
- Câncer colorretal metastático (CCRm) do tipo RAS selvagem;
- Câncer colorretal metastático (CCRm) com mutação KRAS G12C.
Dose: 6 mg/kg
Dose Máxima: 6 mg/kg IV a cada 2 semanas.
Ajuste de dose:
Populações especiais – A segurança e eficácia do VECTIBIX não foram estudadas em pacientes com insuficiência renal ou hepática.
População pediátrica – Não há experiência em crianças e VECTIBIX é contraindicado para pacientes menores de 18 anos.
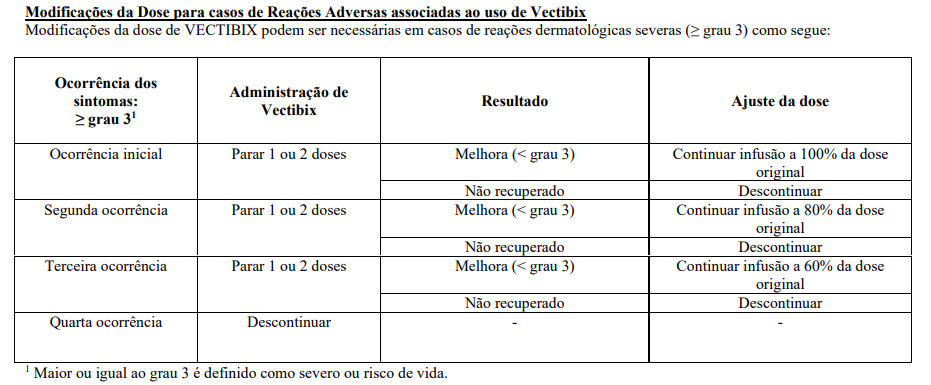
Vias de administração: Intravenosa.
Preparo:
Antes da infusão, o VECTIBIX deverá ser diluído em solução de cloreto de sódio 9 mg/ml (0,9%) para injeção em uma concentração que não deve exceder 10 mg/ml. O VECTIBIX deve ser administrado utilizando um filtro em linha de 0,2 ou 0,22 micrômetros, com baixa capacidade de ligação às proteínas, através de um acesso periférico ou de um cateter de permanência. VECTIBIX é destinado apenas para dose única. VECTIBIX deve ser diluído em cloreto de sódio a 0,9% por um profissional de saúde utilizando técnica asséptica. Não sacuda ou agite o frasco vigorosamente. VECTIBIX deve ser inspecionado visualmente antes da administração. A solução deve ser incolor e pode conter partículas proteináceas, amorfas, translúcidas a brancas visíveis (as quais serão removidas por filtração em linha). Não administrar VECTIBIX se sua aparência não estiver conforme descrição acima. Utilizar somente agulha hipodérmica com um diâmetro menor ou igual a 21 gauges. Retire a quantidade necessária de VECTIBIX para uma dose de 6 mg/kg. Não utilize dispositivos sem agulha (por exemplo: adaptadores de frasco) para retirar o conteúdo do frasco. Dilua em um volume total de 100 mL. A concentração final não deve exceder 10 mg/mL. Doses superiores a 1.000 mg devem ser diluídas em 150 mL de cloreto de sódio a 0,9%. A solução diluída deve ser misturada por inversão suave, não agite.
Administração:
O VECTIBIX deve ser administrado como uma infusão intravenosa por meio de uma bomba de infusão. O tempo de infusão recomendado é de, aproximadamente, 60 minutos. Se a primeira infusão for tolerada, infusões subsequentes podem ser administradas por 30 a 60 minutos. Doses superiores a 1.000 mg devem ser infundidas durante, aproximadamente, 90 minutos. A linha de infusão deve ser irrigada com 0,9% de uma solução de cloreto de sódio antes e após a administração de VECTIBIX para evitar misturar com outros medicamentos ou soluções intravenosas. Pode ser necessária uma redução na taxa de infusão de VECTIBIX em casos de reações relacionadas à infusão. VECTIBIX não deve ser administrado por injeção intravenosa ou em bolus.
Cuidados e orientações:
Devido ao potencial de reações adversas graves em lactentes expostas ao panitumumab, aconselhe as mulheres a interromperem o tratamento. O aleitamento materno é recomendado durante o tratamento e por 2 meses após a última dose. Não se sabe se o panitumumabe está presente no leite materno, embora muitos medicamentos sejam excretados nesse leite. A IgG humana está presente no leite materno, mas dados publicados sugerem que os anticorpos presentes no leite materno não entram na circulação neonatal e infantil em quantidades significativas. Aconselhe os pacientes que recebem panitumumab a usar protetor solar, chapéu e limitar a exposição à luz solar (UV) durante a terapia e por 2 meses após a última dose, pois a exposição aos raios UV pode exacerbar quaisquer reações cutâneas que possam ocorrer.
Interações Medicamentosas:
Bevacizumabe: (Principal). Não utilize panitumumabe com bevacizumabe em combinação com quimioterapia, pois pode ocorrer aumento da mortalidade e da toxicidade. Em uma análise interina de um estudo clínico aberto, multicêntrico e randomizado com pacientes com câncer colorretal metastático não tratado previamente, a combinação de panitumumabe, bevacizumabe e quimioterapia resultou em diminuição da sobrevida global e aumento da incidência de reações adversas de grau 3 a 5 em comparação com bevacizumabe mais quimioterapia sem panitumumabe, incluindo óbitos. Os pacientes randomizados para o braço do panitumumabe também receberam uma intensidade de dose relativa média menor de cada agente quimioterápico (oxaliplatina, irinotecano e 5‑fluorouracilo) durante as primeiras 24 semanas do estudo em comparação com aqueles randomizados para bevacizumabe e quimioterapia.
Estabilidade/ Conservação:
O VECTIBIX não contém nenhum conservante antimicrobiano, nem agente bacteriostático. Deve ser utilizado imediatamente depois da diluição. Se não for utilizado imediatamente, o tempo de armazenamento em uso e as condições antes da utilização são de responsabilidade do usuário e não devem ultrapassar 24 horas a uma temperatura entre 2°C a 8°C. A solução diluída não deve ser congelada.
VECTIBIX é contraindicado em pacientes com história de reações de hipersensibilidade com risco de morte ao princípio ativo ou a qualquer um dos excipientes. Pacientes com pneumonite intersticial ou fibrose pulmonar. A combinação de VECTIBIX com quimioterapia contendo oxaliplatina é contraindicada para pacientes com CCRm com RAS tipo mutado ou para pacientes com CCRm cujo estado de RAS seja desconhecido. Este medicamento é contraindicado para menores de 18 anos, devido à insuficiência de dados de segurança e eficácia.
Reações adversas:
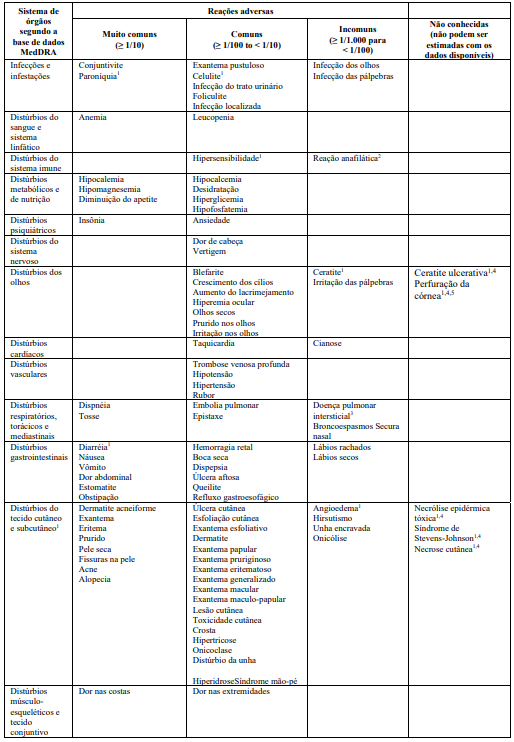

Fonte:
CLINICALKEY. Panitumumab. Monografia farmacológica. Disponível em: <https://www.clinicalkey.com/pharmacology/monograph/3502>. Acesso em: 23 abr. 2026.
BRASIL. Agência Nacional de Vigilância Sanitária (ANVISA). Bulário eletrônico: Vectibix® (panitumumabe). Disponível em: <https://consultas.anvisa.gov.br/#/bulario/q/?nomeProduto=vect>. Acesso em: 23 abr. 2026.
