Nome Comercial/ Apresentação
Abraxane (paclitaxel) 3% / Pó liofilizado para suspensão injetável
Classe Terapêutica
Agente antineoplásico
Indicação
Em combinação com gencitabina, é indicado para o tratamento em primeira linha de pacientes com adenocarcinoma de pâncreas metastático.
Dose
Adenocarcinoma de pâncreas
A dose recomendada é 125 mg/m2, administrada como uma infusão intravenosa durante 30-40 minutos nos Dias 1, 8 e 15 de cada ciclo de 28 dias. A dose recomendada de gencitabina é 1000 mg/m2, administrada como uma infusão intravenosa durante 30-40 minutos iniciando imediatamente após a conclusão da administração de paclitaxel albuminado nos Dias 1, 8 e 15 de cada ciclo de 28 dias.
Ajustes de dose durante o tratamento de adenocarcinoma de pâncreas
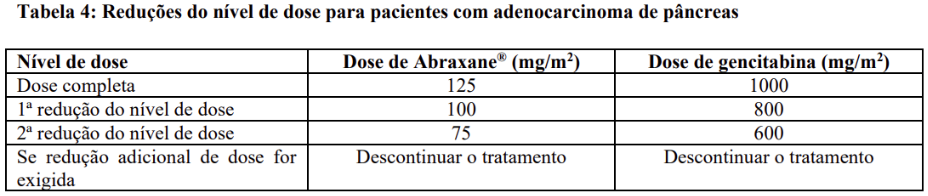
Reduções do nível de dose para pacientes com adenocarcinoma de pâncreas são fornecidas na Tabela 4: Reduções do nível de dose para pacientes com adenocarcinoma de pâncreas.
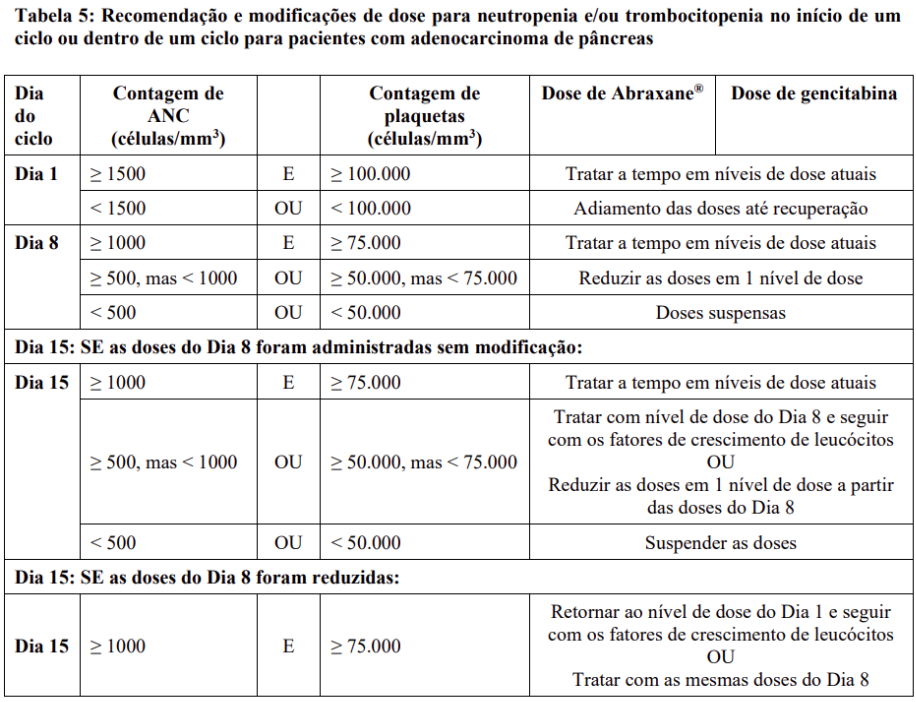
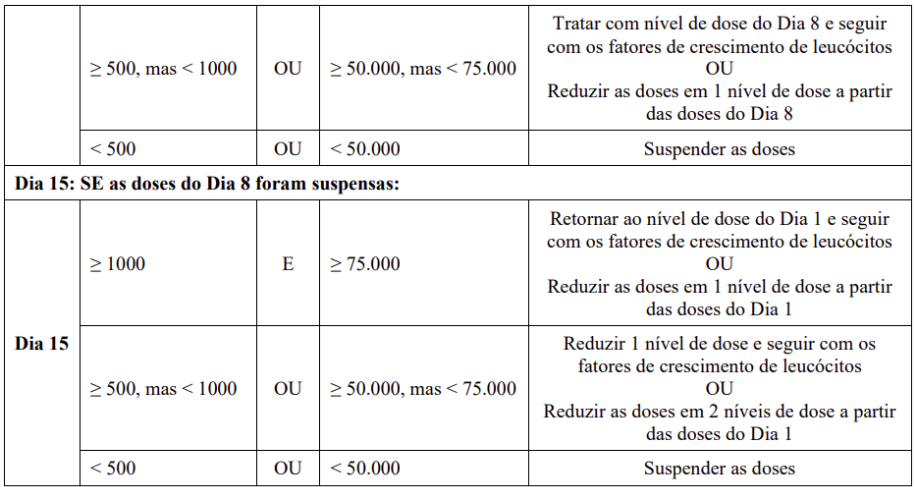
Recomendação e modificações de dose para neutropenia e trombocitopenia no início de um ciclo ou dentro de um ciclo para pacientes com adenocarcinoma de pâncreas são fornecidas na Tabela 5: Recomendação e modificações de dose para neutropenia e/ou trombocitopenia no início de um ciclo ou dentro de um ciclo para pacientes com adenocarcinoma de pâncreas.
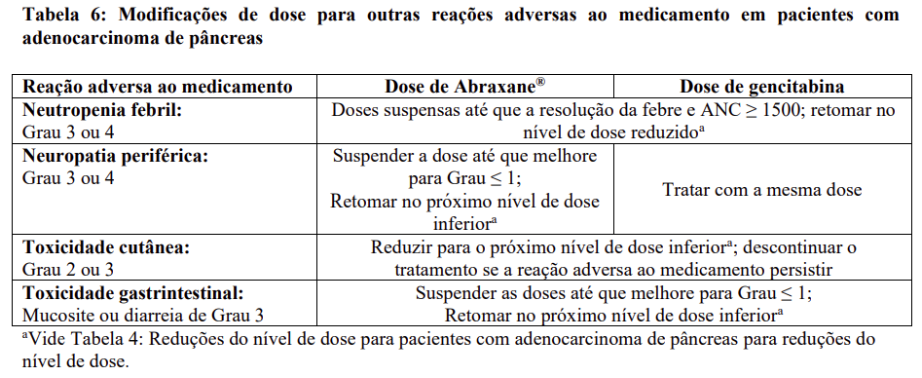
Modificações de dose para outras reações adversas ao medicamento em pacientes com adenocarcinoma de pâncreas são fornecidas na Tabela 6: Modificações de dose para outras reações adversas ao medicamento em pacientes com adenocarcinoma de pâncreas.
Pacientes pediátricos
A segurança e eficácia em crianças (menores de 18 anos) não foram estabelecidas. Portanto, não é recomendada para uso pediátrico.
Idosos
Nenhuma recomendação adicional de dose, exceto aquelas recomendadas para todos os pacientes, é necessária para pacientes com 65 anos ou mais.
Ajuste de dose
Uso em pacientes com função renal comprometida
Ajuste da dose inicial não é exigido para pacientes com comprometimento renal leve a moderado (depuração de creatinina estimada ≥ 30 a < 90 mL/min). Há dados insuficientes para permitir recomendações de dose em pacientes com comprometimento renal grave ou nefropatia em estágio terminal (depuração de creatinina estimada < 30 mL/min).
Uso em pacientes com função hepática comprometida
Para pacientes com comprometimento hepático leve (bilirrubina total > 1 a ≤ 1,5 x LSN e aspartato aminotransferase ≤ 10 x LSN), nenhum ajuste de dose é exigido. Tratar com as mesmas doses indicadas para pacientes com função hepática normal. Há dados insuficientes para permitir recomendações de dose para pacientes com adenocarcinoma de pâncreas metastático que apresentam comprometimento hepático grave. Para pacientes com bilirrubina total > 5 x LSN ou aspartato aminotransferase > 10 x LSN, há dados insuficientes para permitir recomendações de dose.
Preparo
É fornecido como um pó estéril liofilizado para reconstituição antes do uso. Cada mL da formulação reconstituída contém 5 mg/mL de paclitaxel.
Usando uma seringa estéril, injetar lentamente 20 mL da solução de 9 mg/mL de cloreto de sódio para injeção em um frasco-ampola. Direcionar o fluxo da solução na superfície interna do frasco-ampola e levar pelo menos 1 minuto para a introdução. Não injetar a solução diretamente no liofilizado, já que isto resultaria em formação de espuma.
Assim que a adição estiver completa, deixar o frasco-ampola em repouso por no mínimo 5 minutos para garantir o umedecimento adequado da parte sólida. Em seguida, misturar e/ou inverter suavemente e lentamente o frasco-ampola por pelo menos 2 minutos até a completa dissolução de qualquer liofilizado. Evitar a formação de espuma.
Calcular o volume de administração total exato de 5 mg/mL de suspensão exigido para o paciente e retirar lentamente o volume da suspensão reconstituída do frasco-ampola em uma seringa. Injetar a quantidade adequada de Abraxane® reconstituído em uma bolsa de infusão vazia e estéril. O uso de recipientes de solução livre de DEHP [di(2-etilhexil) ftalato] especializados ou conjuntos de administração não são necessários para preparar ou administrar infusões. O uso de dispositivos médicos que contêm óleo de silicone como um lubrificante (ou seja, seringas e bolsas de infusão) para reconstituir e administrar pode resultar na formação de filamentos proteicos.
Inspecionar visualmente a suspensão reconstituída na bolsa de infusão antes da administração. Se forem observados filamentos, administrar a suspensão reconstituída em um filtro de 15 μm.
Não usar um filtro com um tamanho de poro menor do que 15 μm. Medicamentos parenterais devem ser inspecionados visualmente para material particulado e descoloração antes da administração, sempre que a solução e recipiente permitirem.
Vias de administração
INTRAVENOSO
Administração
A suspensão reconstituída deve ser leitosa e homogênea sem partículas visíveis. Se partículas ou sedimentação são visíveis, o frasco-ampola deve ser invertido suavemente novamente para garantir a ressuspensão completa antes do uso.
É um medicamento anticâncer citotóxico e, como com outros compostos de paclitaxel potencialmente tóxicos, deve-se ter cautela ao manipular. É recomendado o uso de luvas. Se (pó liofilizado ou suspensão reconstituída) entrar em contato com a pele, lave-a imediatamente e abundantemente com sabão e água. Após a exposição tópica, eventos podem incluir formigamento, ardor e vermelhidão. Se entrar em contato com membranas mucosas, essas devem ser lavadas abundantemente com água.
Dada a possibilidade de extravasamento, é aconselhável monitorar rigorosamente o local de infusão para possível infiltração durante a administração do medicamento. Limitar a infusão em 30 minutos, conforme orientado, reduz a probabilidade de reações relacionadas à infusão.
Cuidados específicos e monitoramento
Advertências e precauções especiais específicas para Abraxane em combinação com gencitabina
Sepse foi relatada em uma taxa de 5% dos pacientes com ou sem neutropenia que receberam Abraxane em combinação com gencitabina. Complicações devido ao câncer pancreático de base, especialmente obstrução biliar ou presença de stent biliar, foram identificadas como fatores contribuintes significativos. Se um paciente se tornar febril (independente da contagem de neutrófilos), iniciar tratamento com antibióticos de amplo espectro. Para neutropenia febril, suspender paclitaxel e gencitabina até que a febre seja resolvida e contagem absoluta de neutrófilos ≥ 1.500 células/mm3. Em seguida retomar o tratamento em níveis de dose reduzidos.
Pneumonite foi relatada em uma taxa de 4% em combinação com gencitabina. Monitorar os pacientes rigorosamente para sinais e sintomas de pneumonite. Após descartar a etiologia infecciosa e após fazer um diagnóstico de pneumonite, descontinuar permanentemente o tratamento com paclitaxel e gencitabina e iniciar imediatamente o tratamento adequado e medidas de suporte.
Avaliar cuidadosamente os pacientes com 75 anos ou mais quanto a capacidade de tolerar o tratamento. Ter atenção especial com o status de desempenho, comorbidades e risco elevado de infecções.
Gravidez, lactação e fertilidade
Categoria D: Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica. Informe imediatamente seu médico em caso de suspeita de gravidez.
Devido à suspeita de que possa causar defeitos congênitos sérios quando administrado durante a gravidez, as mulheres que utilizam esse medicamento devem ser aconselhadas a usarem métodos contraceptivos altamente eficazes e pelo menos durante seis meses após a última dose administrada desse medicamento.
Pacientes do sexo masculino tratados são aconselhados a usarem um método de contracepção efetivo e evitar engravidar sua parceira durante e até três meses após o tratamento.
Uso na gravidez
Não há estudos adequados e bem controlados em gestantes. Mulheres com potencial de engravidar devem realizar um teste de gravidez antes de iniciar o tratamento.
Se este medicamento for usado durante a gravidez, ou se a paciente engravidar enquanto estiver recebendo este medicamento, a mesma deve ser informada do risco potencial ao feto.
Suspeita-se que causa defeitos congênitos sérios quando administrado durante a gravidez.
Como outros citostáticos genotóxicos, pode ter efeitos genotóxicos.
Uso na lactação
Paclitaxel e/ou seus metabólitos foram excretados no leite de ratas prenhes. Devido ao potencial para reações adversas sérias em lactentes, a lactação deve ser descontinuada durante o tratamento.
Fertilidade
Induziu infertilidade em ratos machos. Com base nos achados em animais, o paclitaxel pode comprometer a fertilidade em fêmeas.
Efeitos sobre a capacidade de dirigir veículos e operar máquinas
Eventos adversos podem afetar a capacidade de dirigir e operar máquinas
Interações medicamentosas
O metabolismo de paclitaxel é catalisado, em parte, pelas isoenzimas CYP2C8 e CYP3A4 do citocromo P450. Portanto, deve-se ter cautela ao administrar concomitantemente com medicamentos conhecidos por inibir (por exemplo, cetoconazol, eritromicina, fluoxetina, antifúngico imidazol, genfibrozila, clopidogrel, cimetidina, ritonavir, saquinavir, indinavir e nelfinavir) ou induzir (por exemplo, rifampicina, carbamazepina, fenitoína, efavirenz, nevirapina) tanto a CYP2C8 ou CYP3A4.
Paclitaxel e gencitabina não compartilham uma via metabólica comum. A depuração do paclitaxel é principalmente determinada pelo metabolismo mediado pela 2C8 e 3A4 do citocromo P450 seguida pela excreção biliar, enquanto gencitabina é inativada pela citidina deaminase seguido pela excreção urinária. As interações farmacocinéticas entre Abraxane e gencitabina não foram avaliadas em humanos.
Estabilidade/ Conservação
Deve ser conservado em temperatura ambiente (temperatura entre 15 e 30⁰C). Manter o frasco ampola dentro de sua embalagem original para protegê-lo da luz.
O congelamento e a refrigeração não afetam negativamente a estabilidade do produto.
Estabilidade da suspensão reconstituída no frasco-ampola
Reconstituído deve ser usado imediatamente, mas pode ser armazenado por até 24 horas a 25ºC, se necessário. Se não usado imediatamente, cada frasco-ampola da suspensão reconstituída deve ser recolocado na embalagem original para protegê-lo da luz. Descartar qualquer porção não utilizada.
Estabilidade da suspensão reconstituída na bolsa de infusão
A suspensão para infusão preparada em uma bolsa de infusão, conforme recomendado, deve ser usada imediatamente, mas pode ser armazenada por até 12 horas a 25ºC e em condições de luminosidade.
Reações adversas
Adenocarcinoma de pâncreas
As estimativas de frequência para reações adversas são definidas como: Muito comum (≥ 1/10); Comum (≥ 1/100 a < 1/10); Incomum (≥ 1/1.000 a < 1/100); Rara (≥ 1/10.000 a < 1/1.000); Muito rara (< 1/10.000) e Desconhecida (não pode ser estimada a partir dos dados disponíveis – relatos espontâneos).
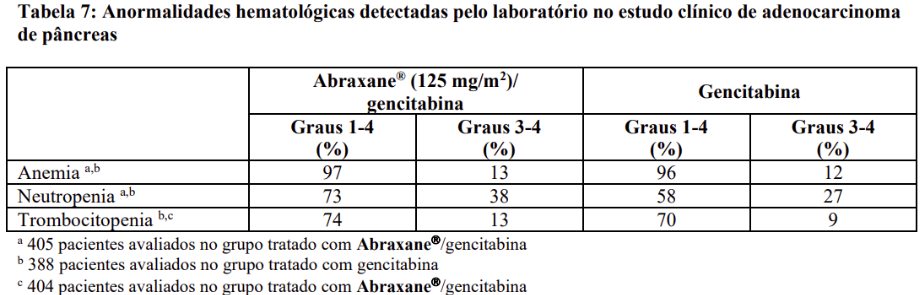
A Tabela 7: Anormalidades hematológicas detectadas pelo laboratório no estudo clínico de adenocarcinoma de pâncreas fornece a frequência e gravidade das anormalidades hematológicas detectadas pelo laboratório para o grupo de Abraxane®/gencitabina e grupo de gencitabina.
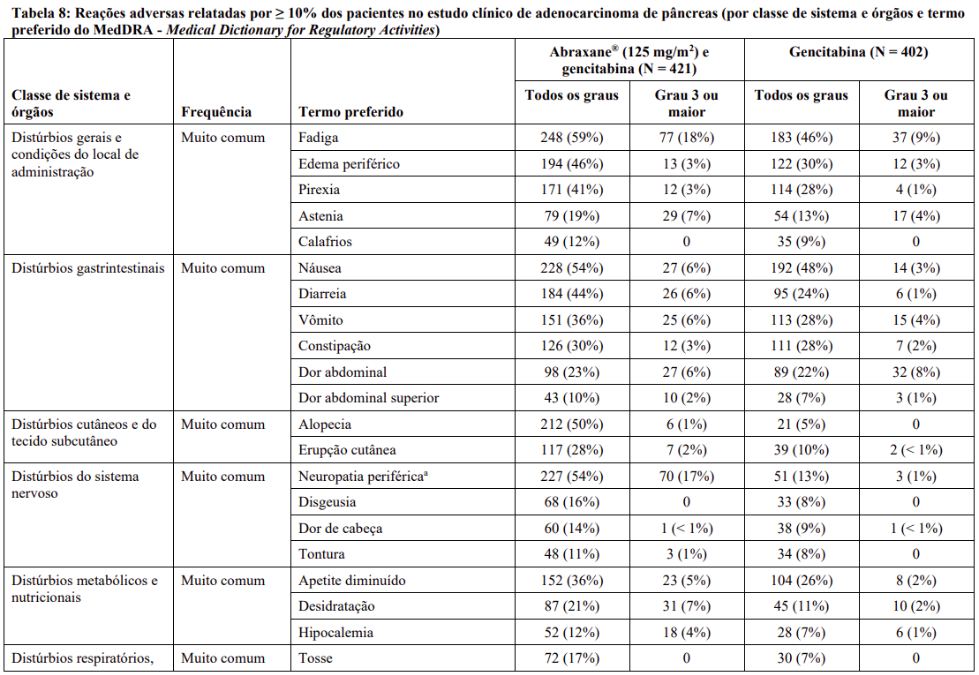
A Tabela 8: Reações adversas relatadas por ≥ 10% dos pacientes no estudo clínico de adenocarcinoma de pâncreas (por classe de sistema e órgãos e termo preferido do MedDRA – Medical Dictionary for Regulatory Activities) fornece a frequência e gravidade de reações adversas por classe de sistema e órgãos/termo preferido que foram relatadas por ≥ 10% dos pacientes com adenocarcinoma de pâncreas que receberam Abraxane® e gencitabina ou monoterapia de gencitabina. Dentro de cada agrupamento de classe de sistema e órgãos, as reações adversas são apresentadas em ordem decrescente de frequência.
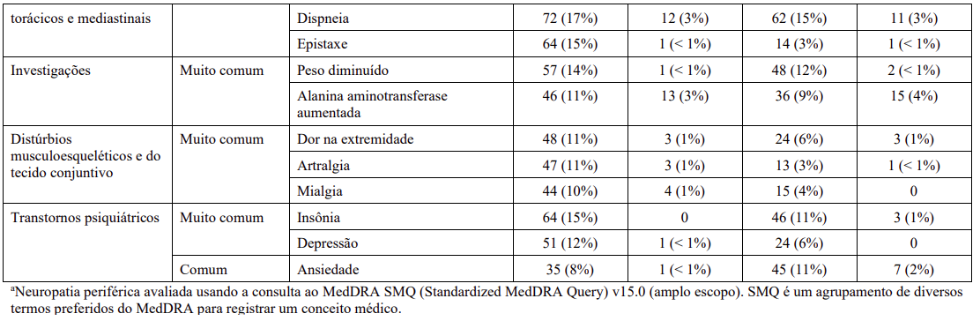
Reações adversas adicionais clinicamente relevantes e que foram relatadas por < 10% dos pacientes com adenocarcinoma de pâncreas que receberam Abraxane®/gencitabina incluíram:
Distúrbios gerais e condições do local da administração: reação no local da infusão (comum)
Distúrbios gastrintestinais: estomatite, boca seca, obstrução intestinal, colite (comum)
Distúrbios cutâneos e do tecido subcutâneo: prurido, pele seca, alteração ungueal, rubor (comum)
Distúrbios do sistema sanguíneo e linfático: pancitopenia (comum), púrpura trombocitopênica trombótica (incomum)
Distúrbios do sistema nervoso: paralisia do nervo VII (incomum)
Distúrbios respiratórios, torácicos e mediastinais: congestão nasal, pneumonitea,1 (comum), garganta seca, ressecamento nasal (incomum)
Infecções e infestações: candidíase oral, pneumonia, sepse (comum) Investigações: aspartato aminotransferase aumentado, bilirrubina sérica aumentada, creatinina sérica aumentada (comum)
Distúrbios musculoesqueléticos e do tecido conjuntivo: dor óssea, fraqueza muscular (comum)
Distúrbios vasculares: hipotensão, hipertensão (comum)
Distúrbios cardíacos: taquicardia, insuficiência cardíaca congestiva (comum)
Distúrbios oftalmológicos: lacrimejamento aumentado (comum), edema macular cistoide (incomum)
Distúrbios hepatobiliares: colangite (comum)
Distúrbios renais e urinários: insuficiência renal aguda (comum), síndrome urêmica hemolítica (incomum)
a Pneumonite é avaliada usando a consulta ao MedDRA SMQ v15.1 de pneumopatia intersticial. SMQ é um agrupamento de diversos termos preferidos do MedDRA para registrar um conceito médico.1
Neuropatia periférica
Para Abraxane® e gencitabina, o tempo mediano para a primeira ocorrência de neuropatia periférica de Grau 3 foi 140 dias, e o tempo mediano para a melhora da neuropatia periférica de Grau 3 a Grau 0 ou 1 foi 29 dias. Dos pacientes com o tratamento interrompido devido à neuropatia periférica, 44% (31/70 pacientes) foram capazes de retomar Abraxane® em uma dose reduzida. Nenhum paciente tratado com Abraxane®/gencitabina apresentou neuropatia periférica de Grau 4.
Sepse
Sepse foi relatada em uma taxa de 5% em pacientes com ou sem neutropenia que receberam Abraxane® em combinação com gencitabina. Complicações devido ao câncer pancreático de base, especialmente obstrução biliar ou presença de stent biliar, foram identificadas como fatores contribuintes significativos. Se um paciente se tornar febril (independente da contagem de neutrófilos), iniciar o tratamento com antibióticos de amplo espectro. Para neutropenia febril, suspender Abraxane® e gencitabina até que a febre seja resolvida e ANC ≥ 1500, em seguida retomar o tratamento em níveis de dose reduzidos.
Pneumonite
Pneumonite foi relatada em uma taxa de 4% com o uso de Abraxane® em combinação com gencitabina. Das 17 reações adversas ao medicamento de pneumonite no braço de Abraxane®/gencitabina, 2 tiveram um resultado fatal. Monitorar os pacientes rigorosamente para sinais e sintomas de pneumonite. Após descartar a etiologia infecciosa e após fazer um diagnóstico de pneumonite, descontinuar permanentemente o tratamento e iniciar imediatamente o tratamento adequado e medidas de suporte.
Reações adversas resultando em morte dentro de 30 dias da última dose da droga em estudo foram relatadas por 4% dos pacientes no grupo de Abraxane® e gencitabina e por 4% dos pacientes no grupo de gencitabina.
Dos 421 pacientes no estudo randomizado que receberam Abraxane® e gencitabina, 41% tinham 65 anos ou mais e 10% tinham 75 anos ou mais. Diarreia, apetite diminuído, desidratação e epistaxe foram mais frequentes em pacientes com 65 anos ou mais em comparação com pacientes com menos de 65 anos de idade. Em pacientes com 75 anos ou mais que receberam Abraxane® e gencitabina, houve uma incidência maior de reações adversas sérias e reações adversas que levaram à descontinuação do tratamento. Avaliar cuidadosamente os pacientes com 75 anos ou mais para a capacidade de tolerar Abraxane® em combinação com gencitabina. Dar consideração especial ao status de desempenho, comorbidades e risco aumentado de infecções.
Câncer de mama metastático
Embora Abraxane® não seja indicado para o tratamento de câncer de mama metastático, eventos cardiovasculares graves, possivelmente relacionados com Abraxane® em monoterapia sob uma dose de 260 mg/m2 a cada 3 semanas, ocorreram em cerca de 3% dos pacientes em um estudo de fase 3. Esses eventos incluíam isquemia cardíaca/infarto, dor torácica, parada cardíaca, taquicardia supraventricular, edema, trombose, tromboembolismo pulmonar, embolia pulmonar e hipertensão. Foram reportados casos de ataques cerebrovasculares (acidente vascular cerebral ou derrame) e ataques isquêmicos transitórios.
Dados pós-comercialização
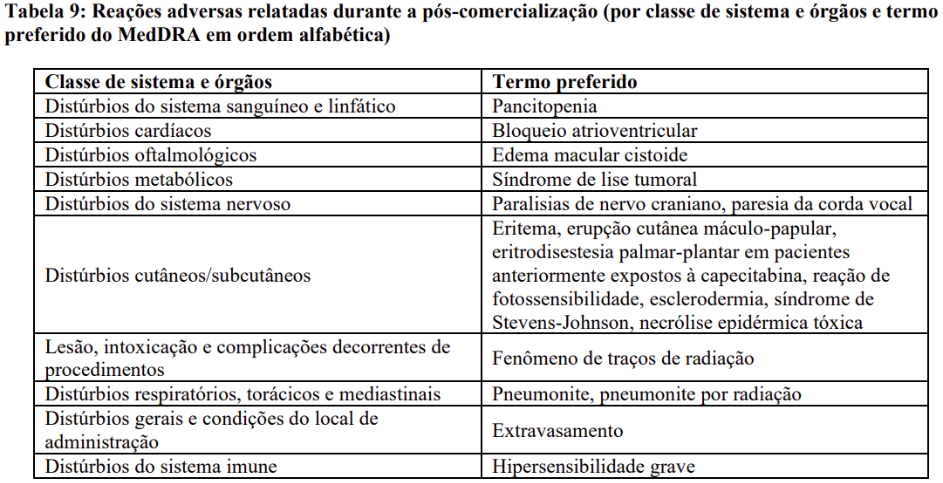
Edema macular cistoide
Houve casos raros relatados (< 1/1000 pacientes) de acuidade visual reduzida devido ao edema macular cistoide durante o tratamento com Abraxane®, bem como com outros taxanos. Espera-se que o edema macular cistoide possa ser resolvido após a cessação do tratamento.
Contraindicações
Não deve ser usado em pacientes que apresentam contagens de neutrófilos basais de < 1.500 células/mm3
É contraindicado em pacientes com hipersensibilidade ao paclitaxel ou à albumina humana.
É contraindicado durante a lactação.
Fonte:
Abraxane®. [Bula]. São Paulo: United Medical Ltda. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=125760033: 25/08/2025
