Nome Comercial e Princípio Ativo / Apresentação:
Zytiga® (Acetato de Abiraterona) 250 mg – Comprimido não revestido
Zytiga® (Acetato de Abiraterona) 500 mg – Comprimido revestido
Classe terapêutica: Antineoplásico – inibidor seletivo da enzima CYP17 (antagonista da síntese de androgênio)
Indicação: Tratamento do câncer de próstata metastático resistente à castração (mCRPC) e câncer de próstata metastático hormônio-sensível (mHSPC) em combinação com ADT e prednisona/prednisolona
Posologia:
Dose recomendada: 1000 mg/dia (2 comp. de 500 mg ou 4 comp. de 250 mg), em tomada única diária
Sempre usar em associação com prednisona/prednisolona.
Dose de prednisona ou prednisolona
Para câncer de próstata metastático não tratado anteriormente com hormônio ou câncer de próstata hormônio-sensível metastático (mHNPC), ZYTIGA® é utilizado com 5 mg de prednisona ou prednisolona diariamente.
Para o câncer da próstata metastático resistente à castração (mCRPC), ZYTIGA® é utilizado com 10 mg de prednisona ou prednisolona diariamente.
Dose máxima: 1000 mg/dia de Zytiga (não deve ser excedida)
Administração: Via oral, em jejum. Tomar pelo menos 2 h após refeição e não ingerir alimentos por 1 h após a dose. Comprimidos devem ser deglutidos inteiros com água.
Não recomendado triturar ou manipular sem orientação
Ajustes de Dose:
Insuficiência hepática: Leve: não requer ajuste. Moderada: usar com cautela, pode ser necessário ajuste. Grave: contraindicado.
Insuficiência renal: Não requer ajuste, mesmo em doença renal grave.
Estabilidade e Conservação:
• Zytiga® 250 mg: válido por 1 mês após aberto.
• Zytiga® 500 mg: válido por 12 semanas após aberto.
• Conservar em embalagem original
Reações adversas:

Antídoto:
Não há antídoto específico. Em caso de superdose → tratamento sintomático e monitoramento de função cardíaca, hepática e eletrólitos.
Contraindicações:
• Gravidez e mulheres em idade fértil
• Insuficiência hepática grave
• Síndrome de má absorção glicose-galactose
Gravidez:
• Categoria X – contraindicado (risco de alterações hormonais fetais).
• Lactação: não indicado; não se sabe se é excretado no leite.
Interações Medicamentosas:
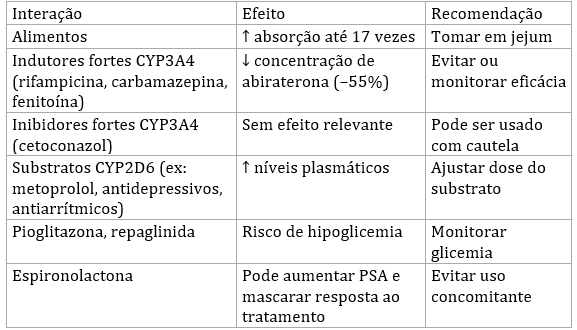
Orientações Extras:
- Monitorar função hepática a cada 2 semanas nos 3 primeiros meses, depois mensalmente.
- Usar preservativo durante relações com parceira grávida; usar preservativo + outro método contraceptivo com mulheres em idade fértil.
- Há risco potências de anemia e disfunção sexual em homens com câncer de próstata
- A pressão arterial, o potássio sérico e a retenção hídrica devem ser monitoradas pelo menos mensalmente. O prolongamento de QT foi observado em pacientes com hipocalemia em associação com o tratamento com ZYTIGA®
- Diminuição da densidade óssea pode ocorrer em homens com câncer de próstata avançado metastático (câncer de próstata resistente à castração). O uso de ZYTIGA® em combinação com um glicocorticoide pode aumentar esse efeito.
- Casos de miopatia e rabdomiólise foram relatados em pacientes tratados com ZYTIGA®. A maioria dos casos foi desenvolvida nos primeiros 6 meses de tratamento e recuperada após a retirada de ZYTIGA®. Recomenda-se precaução em doentes com tratamento concomitante com medicamentos que se sabe serem associados a miopatia/rabdomiólise.
- ZYTIGA® deve ser usado com cautela em pacientes com histórico de doença cardiovascular.
Fonte: Zytiga® [Bula] São Paulo: Janssen-Cilag Farmacêutica Ltda. Disponível em: blob:https://consultas.anvisa.gov.br/61ff3193-165f-40c6-be3f-56867b458735 : 03/09/2024.
