Nome Comercial e Princípio Ativo / Apresentação:
Orencia® (abatacepte) – pó liofilizado para solução injetável 250 mg (frasco-ampola, IV)
Orencia® (abatacepte) – solução injetável SC: seringas preenchidas com 125 mg/1 mL.
Classe terapêutica: Antineoplásico – Modulador de coestimulação seletivo (proteína de fusão CTLA‑4Ig) — imunomodulador biológico.
Indicações: Artrite Reumatoide (adultos), Artrite Idiopática Juvenil (≥6 anos), Artrite Psoriásica (adultos).
Dose:
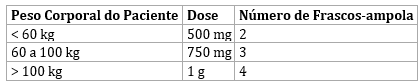
– Observação: Cada frasco-ampola contém 250 mg de abatacepte para administração.
SC: 125 mg 1x/semana (adultos). AIJ – Artrite Idiopática Juvenil (≥6 anos): 10 mg/kg IV (máx. 1000 mg).
Dose máxima:
IV: 1000 mg por administração.
SC: 125 mg por semana (dose fixa, independente do peso).
Ajuste de dose:
Não requer ajuste em insuficiência renal/hepática ou idosos (não estudado).
Pediatria:
Para uso IV: Não recomendados em menores de 6 anos, devido à ausência de dados de segurança e eficácia nessa população.
Para uso SC: Não administrar em pacientes pediátricos com menos de 50kg.
Preparo IV:
Reconstituição: 10mL água para injetáveis (girar suavemente)
Concentração: 25 mg/mL.
Diluição: SF0,9% QSP 100mL.
Tempo de infusão: 30 minutos.
Dispositivo de infusão: bomba de infusão com filtro 0,2 – 1,2 µm
Uso SC: medicamento pronto para uso
Vias de administração: Intravenosa (IV) e Subcutânea (SC).
Estabilidade/ Conservação:
Manter sob refrigeração. SC: usar após atingir temperatura ambiente (~30 min). IV: usar solução reconstituída/diluída imediatamente.
– Se não for usado na hora, a solução pode ser armazenada por até 24 horas entre 2–8 °C (mantendo condições assépticas).
– Não congelar.
Reações adversas:
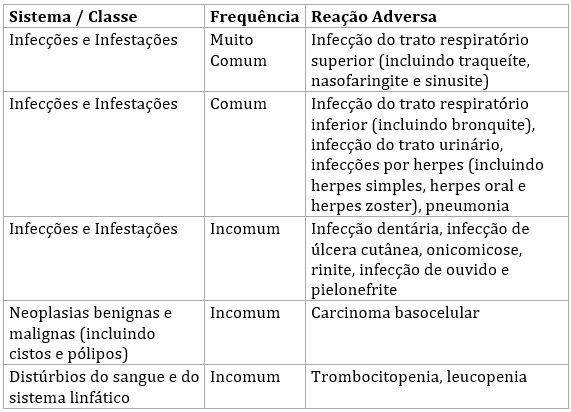
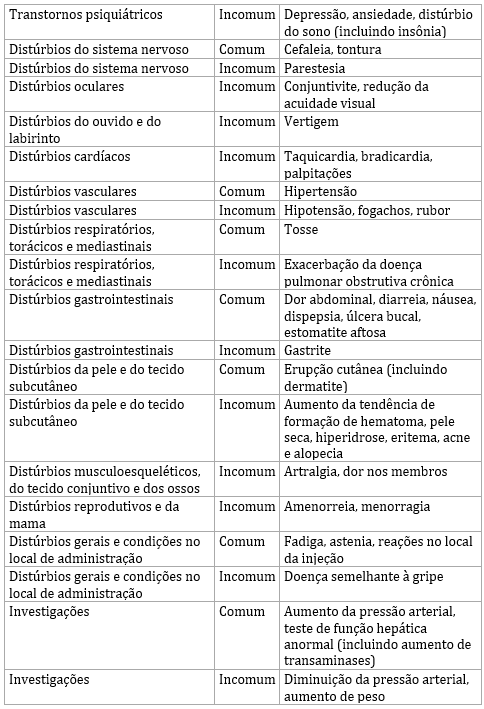
Antídoto: Não há antídoto específico.
Contraindicações: Hipersensibilidade ao abatacepte ou excipientes. Uso concomitante com antagonistas de TNF ou outros biológicos (ex.: anakinra)
Classificação de risco para gestantes: Categoria C (usar apenas se claramente necessário).
Lactação:
O abatacepte pode atravessar a placenta para o soro de crianças nascidas de mulheres tratadas com abatacepte durante a gravidez. Não sendo recomendado a amamentação durante o uso do medicamento.
Interações medicamentosas:
Uso concomitante de abatacepte com medicamentos bloqueadores do TNF (ex: adalimumabe, etanercepte, infliximabe, golimumabe, certolizumabe) está associado a risco aumentado de infecções graves
Não há experiência suficiente para avaliar segurança/eficácia ao usar abatacepte com outros biológicos como anakinra simultaneamente. Portanto, também não recomendado.
Embora poucas evidências específicas, a bula alerta que combinação com agentes que reduzem contagem de linfócitos pode potencializar os efeitos imunomodulatórios do abatacepte, aumentando risco de infecções.
Cuidados e orientações:
Abatacepte IV contém maltose, que pode interferir em medidores de glicose que utilizam reagentes de glicose desidrogenase pirroloquinolina quinona (GDH-PQQ), levando a leituras falsamente elevadas de glicose logo após a infusão. Pacientes diabéticos que fazem automonitoramento devem usar métodos que não reagem com maltose. SC não contém maltose
Vacinas vivas não devem ser administradas concomitantemente com abatacepte ou dentro de 3 meses após sua descontinuação.
Vacinas inativas: abatacepte pode reduzir resposta imune a algumas vacinas (como influenza e pneumocócica)
Fonte: Orencia [Bula]. São Paulo: Bristol-Myers Squibb (BMS). Disponível em: blob:https://consultas.anvisa.gov.br/5313f46b-11ff-4550-bae2-20ce3bf83dfe : 28/06/2024
