Nome Comercial/ Apresentação
Ocrevus (ocrelizumabe) 300 mg/10 mL / Solução para diluição para infusão
Classe Terapêutica
Anticorpo Monoclonal
Indicação
É indicado para o tratamento de pacientes com formas recorrentes de esclerose múltipla (EMR) e de pacientes com esclerose múltipla primária progressiva (EMPP).
Dose
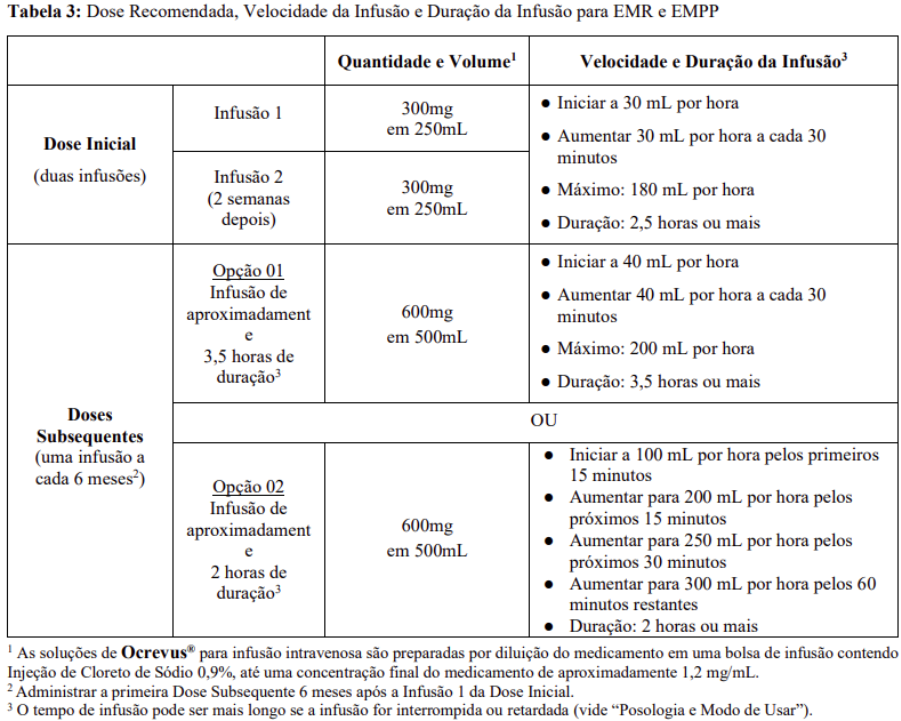
Dosagem recomendada e administração da dose
● Administrar sob rigorosa supervisão de um profissional de saúde experiente com acesso a suporte médico apropriado para controlar reações severas como reações sérias à infusão.
● Dose inicial: infusão intravenosa de 300 mg, seguida, duas semanas depois, por uma segunda infusão intravenosa de 300 mg.
● Doses subsequentes: infusão intravenosa única de 600 mg a cada 6 meses.
● Observar o paciente por pelo menos uma hora após o término da infusão.
Se os pacientes não apresentaram uma reação relacionada à infusão séria com qualquer infusão anterior de Ocrevus®, uma infusão mais curta (2 horas) pode ser administrada para as doses subsequentes (vide tabela 3, opção 2).
Doses postergadas ou omitidas
Se uma infusão planejada for omitida, administrar assim que possível; não aguardar até a próxima dose programada. Redefinir o cronograma de dosagem para administrar a próxima dose sequencial 6 meses depois que a dose omitida for administrada. As doses devem ter um intervalo de pelo menos 5 meses.
Ajuste de dose
Insuficiência renal: não há ajustes de dosagem previstos na bula do fabricante.
Insuficiência hepática: não há ajustes de dosagem previstos na bula do fabricante.
Preparo
Utilize agulha e seringa estéreis para a preparação da solução diluída para infusão. Não é recomendável o uso de dispositivos de transferência de sistema fechado para a preparação, uma vez que não há evidências sobre a compatibilidade desses dispositivos com o produto.
O produto não contém conservantes e se destina a uso único.
Inspecionar visualmente quanto à presença de material particulado e descoloração antes da administração. Não usar a solução se houver descoloração ou se a solução contiver discreta quantidade de material particulado estranho. Não agitar.
Retirar a dose pretendida e diluir em uma bolsa de infusão contendo Injeção de Cloreto de Sódio 0,9%, até uma concentração final do medicamento de aproximadamente 1,2 mg/mL.
● Retirar 10 mL (300 mg) e injetar em 250 mL
● Retirar 20 mL (600 mg) e injetar em 500 mL
Não usar outros diluentes uma vez que seu uso não foi testado. O produto não contém conservantes e destina-se somente a uso único.
A solução para infusão diluída precisa ser administrada usando um equipo de infusão com filtro de linha de 0,2 ou 0,22 mícron.
Antes de iniciar a infusão IV, o conteúdo da bolsa de infusão precisar estar em temperatura ambiente para evitar uma reação de infusão decorrente de aplicação de solução com temperatura baixa.
Vias de administração
INTRAVENOSA
Administração
É uma solução sem conservantes, estéril, clara ou ligeiramente opalescente, e incolor a marrom pálida fornecida em uma caixa contendo uma ampola de dose única de 300 mg/10 mL (30 mg/mL). Antes do início da infusão intravenosa, o conteúdo da bolsa de infusão deve estar em temperatura ambiente.
Utilizar a solução de infusão preparada imediatamente. Se não for usada imediatamente, armazenar até 24 horas no refrigerador entre 2°C–8°C e 8 horas em temperatura ambiente até 25°C, incluindo o tempo de infusão.
Caso a infusão intravenosa não possa ser concluída no mesmo dia, descartar a solução restante.
Cuidados específicos e monitoramento
Reações à Infusão
Prurido, erupção cutânea, urticária, eritema, broncoespasmo, irritação na garganta, dor orofaríngea, dispneia, edema na faringe ou laringe, rubor, hipotensão, pirexia, fadiga, cefaleia, tontura, náusea, taquicardia e anafilaxia. Em estudos clínicos da esclerose múltipla (EM), a incidência de reações à infusão em pacientes tratados com Ocrevus®, que receberam metilprednisolona (ou um esteroide equivalente) e possivelmente outra pré-medicação para reduzir o risco de reações à infusão antes de cada infusão, foi de 34 a 40%, sendo a incidência mais alta com a primeira infusão. Não houve nenhuma reação à infusão fatal, mas 0,3% dos pacientes com EM tratados com Ocrevus® apresentaram reações à infusão que foram sérias, algumas com necessidade de hospitalização.
Observar os pacientes tratados com Ocrevus® quanto à presença de reações à infusão durante a infusão e por pelo menos uma hora após o término da infusão. Informar os pacientes que reações à infusão podem ocorrer até 24 horas após a infusão.
Reduzindo o risco de reações à infusão e tratando as reações à infusão
Administrar a pré-medicação (ex. metilprednisolona ou um corticosteroide equivalente, e um anti-histamínico) para reduzir a frequência e a gravidade de reações à infusão. A adição de um antipirético (ex. acetaminofeno) também pode ser considerada.
As recomendações de tratamento das reações à infusão dependem do tipo e da gravidade da reação. Para reações à infusão de risco à vida, interromper imediata e permanentemente o uso de Ocrevus® e administrar o tratamento de suporte apropriado. Para reações à infusão menos severas, o tratamento pode envolver a interrupção temporária da infusão, redução da velocidade de infusão e/ou administração de tratamento sintomático.
Infecções
Infecções graves bacterianas, virais, parasitárias e fúngicas, incluindo infecções de risco à vida ou fatais, foram reportadas em pacientes tratados com Ocrevus®. Um risco maior de infecções (incluindo infecções graves e fatais, bacterianas, fúngicas e virais nova ou de vírus reativado) foi observado em pacientes durante e após a finalização do tratamento com terapias antiCD20 que depletam células B.
Uma proporção maior de pacientes tratados com Ocrevus® apresentou infecções em comparação com pacientes que usaram REBIF ou placebo. Nos estudos de EMR, 58% dos pacientes tratados com Ocrevus® apresentaram uma ou mais infecções em comparação com 52% dos pacientes tratados com REBIF. No estudo de EMPP, 70% dos pacientes tratados com Ocrevus® apresentaram uma ou mais infecções em comparação com 68% dos pacientes com placebo. Ocrevus® aumentou o risco de infecções do trato respiratório superior, infecções do trato respiratório inferior, infecções cutâneas e infecções relacionadas a herpes.
Ocrevus® não esteve associado a um aumento no risco de infecções sérias em pacientes com EM nos estudos controlados.
Postergar a administração em pacientes com uma infecção ativa até que a infecção seja resolvida.
Em caso de suspeita de dengue, ou quando associado a outros medicamentos que aumentem o efeito hemorrágico, a prescrição deste medicamento ou a manutenção do tratamento com ele deve ser reavaliada, devido a seu potencial hemorrágico.
Infecções do trato respiratório
Uma proporção maior de pacientes tratados com Ocrevus® apresentou infecções do trato respiratório em comparação com pacientes que usaram REBIF ou placebo. Nos estudos de EMR, 40% dos pacientes tratados com Ocrevus® apresentaram infecções do trato respiratório superior em comparação com 33% dos pacientes tratados com REBIF, e 8% dos pacientes tratados com Ocrevus® apresentaram infecções do trato respiratório inferior em comparação com 5% dos pacientes tratados com REBIF. No estudo de EMPP, 49% dos pacientes tratados com Ocrevus® apresentaram infecções do trato respiratório superior em comparação com 43% dos pacientes com placebo e 10% dos pacientes tratados com Ocrevus® apresentaram infecções do trato respiratório inferior em comparação com 9% dos pacientes com placebo. As infecções foram predominantemente leves a moderadas e consistiam, sobretudo em infecções do trato respiratório superior e bronquite.
Medicamentos imunossupressores podem ativar focos primários de tuberculose. Esteja alerta quanto à possibilidade de surgimento de doença ativa, tomando os cuidados para o diagnóstico precoce e tratamento.
Herpes
Em estudos clínicos controlados por medicamento ativo (EMR), infecções por herpes foram relatadas de forma mais frequente em pacientes tratados com Ocrevus® do que em pacientes tratados com REBIF, incluindo herpes zoster (2,1% vs. 1,0%), herpes simples (0,7% vs. 0,1%), herpes oral (3,0% vs. 2,2%), herpes genital (0,1% vs. 0%), e infecção pelo vírus do herpes (0,1% vs. 0%). As infecções foram de gravidade predominantemente leve a moderada.
No estudo clínico controlado por placebo (EMPP), herpes oral foi relatada com maior frequência nos pacientes tratados com Ocrevus® do que nos pacientes com placebo (2,7% vs 0,8%).
Casos graves de infecções causadas pelo vírus do herpes simples e varicela-zoster, incluindo infecções do sistema nervoso central (encefalite e meningite), infecções intraoculares e infecções disseminadas na pele e tecidos moles, foram reportados no período pós-comercialização em pacientes com esclerose múltipla tratados com Ocrevus®.
Infecções sérias causadas pelo vírus do herpes podem ocorrer a qualquer momento durante o tratamento com Ocrevus®. Alguns casos reportados apresentaram risco de morte.
Caso ocorra infecção grave causada pelo vírus do herpes, Ocrevus® deve ser descontinuado ou interrompido até que a infecção esteja resolvida, e tratamento adequado deve ser administrado.
Reativação do Vírus da Hepatite B (HBV)
A reativação do vírus da hepatite B foi relatada em pacientes com esclerose múltipla tratados com Ocrevus® no período pós comercialização. Hepatite fulminante, insuficiência hepática e morte causadas pela reativação do HBV ocorreram em pacientes tratados com anticorpos anti-CD20. Realizar o teste de HBV em todos os pacientes antes do início do tratamento com Ocrevus®. Não administrar Ocrevus® a pacientes com HBV ativo confirmado por resultados positivos nos testes de HBsAg e anti-HB. Para pacientes negativos para o antígeno de superfície [HBsAg] e positivos para o anticorpo antinuclear de HB [HBcAb+] ou que são portadores de HBV [HBsAg+], consultar um especialista em doença hepática antes de iniciar e durante o tratamento.
Possível risco aumentado de efeitos imunossupressores com outros imunossupressores
Ao iniciar Ocrevus® após uma terapia imunossupressora ou ao iniciar uma terapia imunossupressora após Ocrevus®, considerar o potencial de efeitos imunossupressores aumentados. Ocrevus® não foi estudado em combinação com outras terapias para EM.
Vacinações
Administrar todas as imunizações de acordo com as diretrizes de imunização pelo menos 4 semanas antes do início de Ocrevus® para vacinas vivas ou vivas atenuadas e, sempre que possível, pelo menos 2 semanas antes do início do tratamento com Ocrevus® para vacinas inativas.
Ocrevus® pode interferir na eficácia de vacinas inativas.
A segurança de imunização com vacinas vivas ou vivas-atenuadas após a terapia com Ocrevus® não foi estudada, e a vacinação com vacinas vivas-atenuadas ou vivas não é recomendada durante o tratamento e até a repleção das células B.
Não há nenhum dado disponível sobre os efeitos de vacina viva ou inativa em pacientes que receberam Ocrevus®.
Vacinação de crianças nascidas de mães tratadas com Ocrevus® durante a gravidez
Não devem ser administradas vacinas vivas ou vivas atenuadas a bebês de mães expostas a Ocrevus® durante a gravidez antes de se confirmar a recuperação das contagens de células B, conforme medido pelo nível de células B, CD19 +. A depleção de células B nestas crianças pode aumentar os riscos relacionados às vacinas vivas ou vivas atenuadas.
Vacinas inativas podem ser administradas antes da recuperação da depleção de células B, conforme indicado, mas deve-se considerar a avaliação das respostas imunológicas da vacina, por meio de consulta com um especialista qualificado, para avaliar se uma resposta imune protetora foi desenvolvida.
Leucoencefalopatia Multifocal Progressiva (LEPM)
Casos de Leucoencefalopatia Multifocal Progressiva (LEMP) foram relatados em pacientes com Esclerose Múltipla tratados com Ocrevus® no período pós-comercialização. A LEMP é uma infecção viral oportunista do cérebro causada pelo vírus JC (JCV) que normalmente ocorre apenas em pacientes imunocomprometidos e que geralmente leva à morte ou incapacidade grave. A LEMP ocorreu em pacientes tratados com Ocrevus® que não haviam sido tratados anteriormente com natalizumabe (que tem uma associação conhecida com LEMP), não estavam tomando quaisquer medicamentos imunossupressores ou imunomoduladores associados ao risco de LEMP antes ou concomitantemente com Ocrevus® e não tinham quaisquer condições médicas sistêmicas conhecidas que resultem em função do sistema imunológico comprometida.
A infecção por JCV resultando em LEMP também foi observada em pacientes tratados com outros anticorpos anti-CD20 e outras terapias para Esclerose Múltipla.
Ao primeiro sinal ou sintoma sugestivo de LEMP, suspenda Ocrevus® e realize uma avaliação diagnóstica apropriada. Os sintomas típicos associados à LEMP são diversos, progridem ao longo de dias a semanas e incluem fraqueza progressiva em um lado do corpo ou falta de jeito dos membros, distúrbios da visão e alterações no pensamento, memória e orientação, levando a confusão e alterações de personalidade.
Os achados de ressonância magnética podem ser aparentes antes dos sinais ou sintomas clínicos. Casos de LEMP, diagnosticados com base em achados de ressonância magnética e na detecção de DNA de JCV no líquido cefalorraquidiano na ausência de sinais ou sintomas clínicos específicos de LEMP, foram relatados em pacientes tratados com outros medicamentos para Esclerose Múltipla associados a LEMP. Muitos desses pacientes posteriormente se tornaram sintomáticos com LEMP. Portanto, o monitoramento com ressonância magnética para sinais que possam ser consistentes com LEMP pode ser útil, e quaisquer achados suspeitos devem levar a uma investigação mais aprofundada para permitir um diagnóstico precoce de LEMP, se presente. Após a descontinuação de outro medicamento para Esclerose Múltipla associado à LEMP, foram relatadas menores mortalidade e morbidade relacionadas à LEMP em pacientes que eram inicialmente assintomáticos no momento do diagnóstico em comparação com pacientes que apresentavam sinais e sintomas clínicos característicos no momento do diagnóstico.
Não se sabe se essas diferenças são devido à detecção precoce e descontinuação do tratamento da Esclerose Múltipla ou devido a diferenças na doença nesses pacientes.
Se a LEMP for confirmada, o tratamento com Ocrevus® deve ser descontinuado
Redução de imunoglobulinas
Conforme esperado com qualquer terapia de depleção de células B, uma redução dos níveis de imunoglobulina é observada no tratamento com Ocrevus®. Os dados agrupados de estudos clínicos de Ocrevus® (EMR e EMPP) e de sua fase aberta open-label (até aproximadamente 7 anos de exposição ao Ocrevus®) demostraram uma associação entre níveis reduzidos de imunoglobulina G (IgG <LIN) e aumento de taxas de infecções graves recorrentes. Considere descontinuar a terapia em paciente com infecções oportunistas sérias ou recorrentes, e se a hipogamaglobulinemia prolongada exigir tratamento com imunoglobulinas intravenosas.
Malignidades
Pode existir um risco maior de malignidade com Ocrevus®. Em estudos controlados, malignidades, incluindo câncer de mama, ocorreram de forma mais frequente em pacientes tratados com Ocrevus®. Câncer de mama ocorreu em 6 de 781 mulheres tratadas com Ocrevus® e nenhuma das 668 mulheres tratadas com REBIF ou placebo. As pacientes devem seguir as diretrizes padrão de triagem de câncer de mama.
Colite imunomediada
Colite imunomediada, que pode se apresentar como uma forma grave e de início agudo de colite, foi relatada em pacientes que receberam Ocrevus® no cenário pós-comercialização. Alguns casos de colite foram graves, necessitando de hospitalização, com alguns pacientes necessitando de intervenção cirúrgica. Corticosteróides sistêmicos foram necessários em muitos desses pacientes. O tempo desde o início do tratamento até o início dos sintomas nesses casos variou de algumas semanas a anos.
Monitore os pacientes para colite imunomediada durante o tratamento com Ocrevus® e avalie imediatamente se ocorrerem sinais e sintomas que possam indicar colite imunomediada, como diarreia nova ou persistente ou outros sinais e sintomas gastrointestinais.
Uso em populações especiais
Gravidez
Ocrevus® é um anticorpo monoclonal humanizado de uma imunoglobulina do subtipo G1. As imunoglobulinas são conhecidas por atravessarem a barreira placentária. Não há dados adequados sobre o risco no desenvolvimento associado ao uso de Ocrevus® por mulheres grávidas. No entanto, depleção transitória de células B periféricas e linfocitopenia foram relatadas em bebês nascidos de mães expostas a outros anticorpos anti-CD20 durante a gravidez. Os níveis de células B em bebês após a exposição materna ao Ocrevus® não foram estudados em ensaios clínicos. A duração potencial da depleção de células B em tais bebês e o impacto da depleção de células B na segurança e eficácia são desconhecidos.
Após a administração de ocrelizumabe a macacas prenhas em doses semelhantes a ou maiores do que as doses usadas clinicamente, observou-se aumento da mortalidade perinatal, depleção de populações de células B, toxicidade renal, da medula óssea e testicular nos filhotes, na ausência de toxicidade materna.
Na população geral dos EUA, o risco inicial estimado de defeitos congênitos significativos e aborto em gestações clinicamente reconhecidas é de 2% a 4% e 15% a 20%, respectivamente. O risco inicial de defeitos congênitos significativos e aborto para a população indicada é desconhecido.
Categoria de risco na gravidez: C. Este medicamento não deve ser utilizado por mulheres grávidas sem orientação médica ou do cirurgião-dentista.
Lactação
Não há dados sobre a presença de ocrelizumabe no leite humano, os efeitos no lactente, ou os efeitos do medicamento na produção de leite. Ocrelizumabe foi excretado no leite de macacas tratadas com ocrelizumabe. IgG humano é excretado no leite humano, e o potencial de absorção de ocrelizumabe para causar depleção de células B no bebê é desconhecido. Os benefícios da amamentação no desenvolvimento e na saúde devem ser considerados juntamente com a necessidade clínica de Ocrevus® da mãe e com qualquer possível efeito adverso no lactente decorrente de Ocrevus® ou da condição subjacente materna.
Uso criterioso no aleitamento ou na doação de leite humano.
O uso deste medicamento no período da lactação depende da avaliação e acompanhamento do seu médico ou cirurgião-dentista.
Mulheres e homens com potencial reprodutivo
Contracepção
Mulheres com potencial para engravidar devem usar um contraceptivo efetivo enquanto estiverem recebendo Ocrevus® e por 6 meses após a última infusão.
Uso pediátrico
A segurança e eficácia em pacientes pediátricos não foi estabelecida.
Uso geriátrico
Estudos clínicos não incluíram quantidades suficientes de indivíduos com idade de 65 ou mais para determinar se eles respondem de forma diferente de indivíduos mais jovens.
Insuficiência renal
Pacientes com comprometimento renal leve foram incluídos nos estudos clínicos. Nenhuma alteração significativa na farmacocinética foi observada nesses pacientes.
Insuficiência hepática
Pacientes com comprometimento hepático leve foram incluídos em estudos clínicos. Nenhuma alteração significativa na farmacocinética foi observada nesses pacientes.
Efeitos sobre a capacidade para dirigir veículos ou operar máquinas
Não possui nenhuma influência, ou possui influência insignificante, na habilidade de dirigir veículos ou operar máquinas.
Até o momento, não há informações de que ocrelizumabe possa causar doping
Interações medicamentosas
Terapias imunossupressoras ou imunomoduladoras
Presume-se que o uso concomitante com outras terapias imunomoduladoras ou imunossupressoras, incluindo doses imunossupressoras de corticosteroides, aumente o risco de imunossupressão. Considerar o risco de efeitos cumulativos no sistema imunológico ao administrar concomitantemente terapias imunossupressoras com Ocrevus®. Ao trocar de medicamentos com efeitos imunológicos prolongados, como daclizumabe, fingolimode, natalizumabe, teriflunomida ou mitoxantrona, considerar a duração e o modo de ação desses medicamentos por causa dos efeitos imunossupressores cumulativos ao iniciar Ocrevus®.
Vacinações
Um estudo aberto, randomizado de Fase 3b, avaliou o uso concomitante de Ocrevus® e várias vacinas inativadas, em adultos entre 18 e 55 anos de idade com formas recorrentes de esclerose múltipla (68 indivíduos em tratamento com Ocrevus® no momento da vacinação e 34 indivíduos não submetidos a tratamento com Ocrevus® no momento da vacinação). A exposição concomitante atenuou as respostas de anticorpos contra a vacina contendo toxóide tetânico, polissacarídeo pneumocócico, vacinas conjugadas pneumocócicas e vacinas contra influenza sazonais inativadas. O impacto da atenuação observada na eficácia da vacina nesta população de pacientes é desconhecido. A segurança e a eficácia das vacinas vivas ou atenuadas administradas concomitantemente com Ocrevus® não foram avaliadas.
Estabilidade/ Conservação
Deve ser conservado sob refrigeração (entre 2 – 8°C). Manter o frasco-ampola dentro do cartucho para proteger da luz. Não congelar. Não agitar.
Reações adversas
Infecções do trato respiratório superior
Reação a infusão
Infecções cutâneas
Infecções do trato respiratório inferior
Dor nas costas
Tosse
Diarreia
Edema periférico
Infecções associadas ao vírus da herpes
Dor nas extremidades
Distúrbios gastrointestinais: colite imunomediada.
Infecções e Infestações: Infecções graves causadas pelo vírus do herpes, leucoencefalopatia multifocal progressiva e babesiose
Pele: Pioderma gangrenoso.
Contraindicações
Ocrevus® é contraindicado para pacientes com:
● Infecção por HBV ativa.
● Histórico de reação à infusão de risco à vida ao Ocrevus®.
● Hipersensibilidade conhecida ao ocrelizumabe ou qualquer de seus excipientes.
Fonte:
Ocrevus ®. [Bula]. São Paulo: Produtos Roche Químicos e Farmacêuticos S.A. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=101000666: 19/08/2025
