Nome Comercial/ Apresentação
Opdivo (nivolumabe) 10mg/mL / Solução injetável
Classe Terapêutica
Anticorpo monoclonal
Indicação
- Melanoma Avançado (Irressecável ou Metastático)
OPDIVO® (nivolumabe) é indicado em monoterapia ou em combinação com ipilimumabe para o tratamento de melanoma avançado (irressecável ou metastático).1
- Tratamento Adjuvante de Melanoma
OPDIVO® (nivolumabe) é indicado para o tratamento adjuvante de adultos com melanoma com envolvimento de linfonodos ou doença metastática completamente ressecada.1 OPDIVO® (nivolumabe) é indicado para o tratamento adjuvante de pacientes adultos e pediátricos (12 anos de idade ou mais) com melanoma, estadio IIB e IIC, que foram submetidos à ressecção cirúrgica completa.1
- Câncer de Pulmão de Células Não Pequenas (CPCNP)
OPDIVO® (nivolumabe) em combinação com quimioterapia dupla à base de platina é indicado para o tratamento neoadjuvante de pacientes adultos com câncer de pulmão de células não pequenas (CPCNP) ressecável (tumores ≥4 cm ou nódulo positivo).2
OPDIVO® (nivolumabe) em combinação com quimioterapia dupla à base de platina como tratamento neoadjuvante, seguido de OPDIVO® (nivolumabe) em monoterapia como tratamento adjuvante após ressecção cirúrgica é indicado para o tratamento de pacientes adultos com CPCNP ressecável (tumores ≥4 cm ou nódulo positivo), e sem mutações EGFR ou rearranjos de ALK conhecidos.2
OPDIVO® (nivolumabe) em combinação com ipilimumabe e 2 ciclos de quimioterapia à base de platina é indicado para o tratamento de primeira linha de CPCNP metastático em adultos cujos tumores não têm mutação EGFR sensibilizante ou translocação de ALK.2
OPDIVO® (nivolumabe) é indicado para o tratamento de CPCNP localmente avançado ou metastático com progressão após quimioterapia à base de platina. Pacientes com mutação EGFR ou ALK devem ter progredido após tratamento com anti-EGFR e anti-ALK antes de receber OPDIVO®. 2
- Carcinoma de Células Renais Avançado (CCR)
OPDIVO® (nivolumabe) é indicado para o tratamento de carcinoma de células renais (CCR) avançado após terapia antiangiogênica prévia.3
OPDIVO® (nivolumabe) em combinação com ipilimumabe é indicado para o tratamento em primeira linha de pacientes adultos com CCR avançado ou metastático que possuem risco intermediário ou alto (desfavorável).3
OPDIVO® (nivolumabe) em combinação com cabozantinibe é indicado para o tratamento em primeira linha de pacientes adultos com CCR avançado.3
- Linfoma de Hodgkin Clássico (LHc)
OPDIVO® (nivolumabe) é indicado para o tratamento de pacientes adultos com Linfoma de Hodgkin clássico (LHc) em recidiva ou refratário após transplante autólogo de células-tronco (TACT) seguido de tratamento com brentuximabe vedotina.4
- Carcinoma de Células Escamosas de Cabeça e Pescoço (CCECP)
OPDIVO® (nivolumabe) é indicado para o tratamento de pacientes com carcinoma de células escamosas de cabeça e pescoço (CCECP) recorrente ou metastático, com progressão da doença durante ou após terapia à base de platina.5
- Carcinoma Urotelial (CU)
OPDIVO® (nivolumabe), em combinação com quimioterapia à base de cisplatina, é indicado para o tratamento em primeira linha de pacientes adultos com carcinoma urotelial irressecável ou metastático.6
OPDIVO® (nivolumabe) é indicado para o tratamento de pacientes com carcinoma urotelial (CU) localmente avançado irressecável ou metastático após terapia prévia à base de platina.6
OPDIVO® (nivolumabe) é indicado para o tratamento adjuvante de pacientes com carcinoma urotelial músculo-invasivo (CUMI) que apresentam alto risco de recorrência após serem submetidos à ressecção radical do tumor.6
- Carcinoma de Células Escamosas do Esôfago (CCEE)
OPDIVO® (nivolumabe) é indicado para o tratamento de carcinoma de células escamosas do esôfago (CCEE) irressecável avançado ou metastático após quimioterapia prévia à base de fluoropirimidina e platina.7
OPDIVO® (nivolumabe), em combinação com quimioterapia contendo fluoropirimidina e platina, é indicado para o tratamento em primeira linha de pacientes adultos com CCEE irressecável avançado, recorrente ou metastático, cujos tumores expressam PD-L1 ≥ 1%.7
OPDIVO® (nivolumabe), em combinação com ipilimumabe, é indicado para o tratamento em primeira linha de pacientes adultos com CCEE irressecável avançado, recorrente ou metastático, cujos tumores expressam PD-L1 ≥ 1%.7
- Tratamento adjuvante de Câncer Esofágico ou de Câncer da Junção Gastroesofágica, completamente ressecados (CE, CJEG)
OPDIVO® (nivolumabe) é indicado para o tratamento adjuvante do câncer esofágico (CE) ou câncer da junção gastroesofágica (CJEG), completamente ressecados, em pacientes que apresentem doença patológica residual após tratamento com quimiorradioterapia (QRT) neoadjuvante.7,10
- Carcinoma Hepatocelular (CHC)
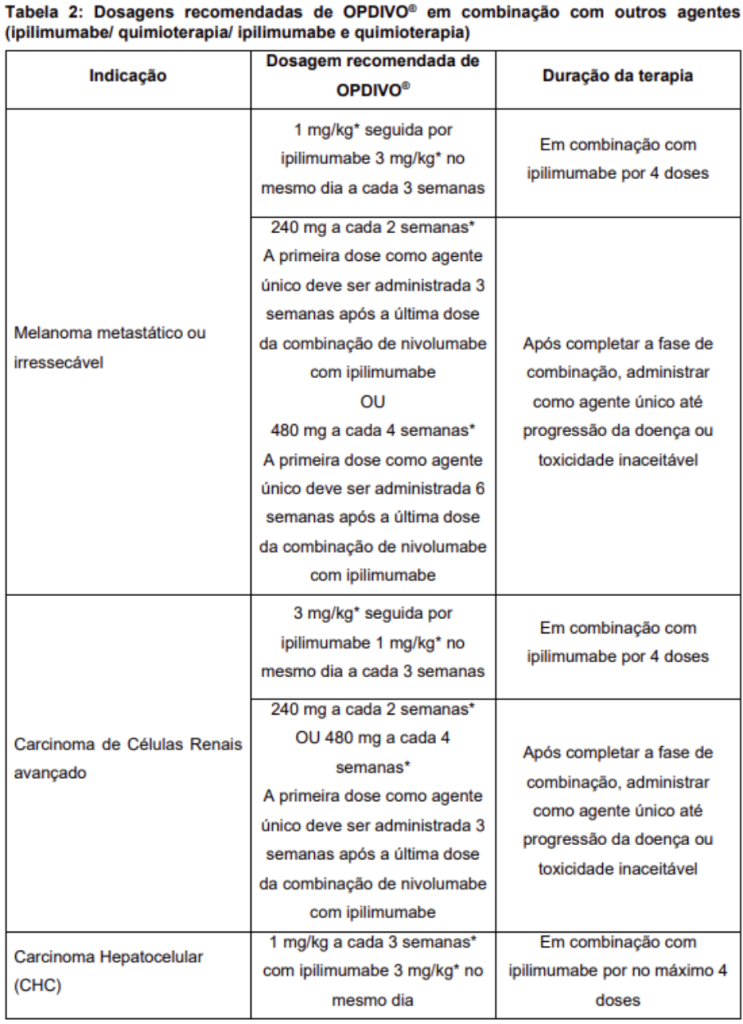
OPDIVO® (nivolumabe), em combinação com ipilimumabe, é indicado para o tratamento em primeira linha de pacientes adultos com carcinoma hepatocelular (CHC) irressecável ou avançado.8
OPDIVO® (nivolumabe), em combinação com ipilimumabe, é indicado para o tratamento de pacientes com carcinoma hepatocelular (CHC) que foram tratados anteriormente com sorafenibe e que não são elegíveis ao tratamento com regorafenibe ou ramucirumabe.8
- Mesotelioma Pleural Maligno (MPM)
OPDIVO® (nivolumabe) em combinação com ipilimumabe é indicado para o tratamento em primeira linha de pacientes adultos com mesotelioma pleural maligno (MPM) irressecável.9
- Câncer Gástrico, Câncer da Junção Gastroesofágica e Adenocarcinoma Esofágico (CG, CJEG, ACE)
OPDIVO® (nivolumabe), em combinação com quimioterapia contendo fluoropirimidina e platina, é indicado para o tratamento de pacientes com câncer gástrico (CG), câncer da junção gastroesofágica (CJEG) e adenocarcinoma esofágico (ACE), avançado ou metastático.10
- Câncer colorretal (CRC)
OPDIVO® (nivolumabe), em combinação com ipilimumabe, é indicado para o tratamento de pacientes adultos e pediátricos com 12 anos ou mais com câncer colorretal (CRC) irressecável ou metastático com alta instabilidade de microssatélites (MSI-H) ou deficiência no reparo de DNA (dMMR).11
1CID C43 – Melanoma maligno da pele; 2CID C34 – Neoplasia maligna dos brônquios e do pulmão; 3CID C64 – Neoplasia maligna do rim, exceto pelve renal; 4CID C81 – Linfoma de Hodgkin; 5CID C76 – Neoplasia maligna da cabeça, face e pescoço; 6CID C67 – Neoplasia maligna da bexiga; 7CID C15 – Neoplasia maligna de esôfago; 8CID C22 – Carcinoma Hepatocelular; 9CID C45 – Mesotelioma pleural maligno; 10CID C16 – Neoplasia maligna do estômago, 11CID C18 – Neoplasia maligna do cólon
Dose
Cálculo da dose
Mais de um frasco de OPDIVO® concentrado poderá ser necessário para gerar a dose total para o paciente.
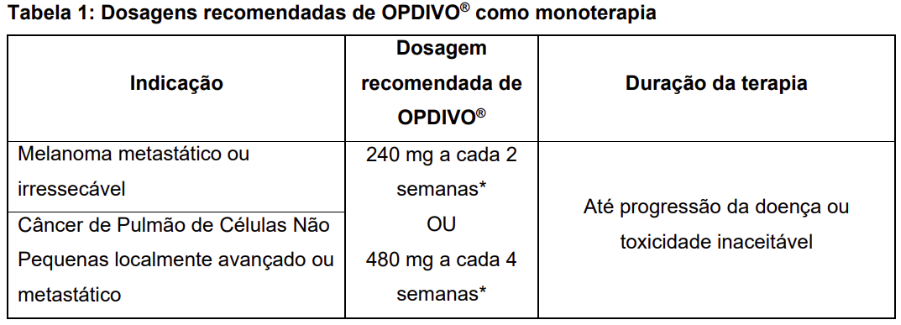
Quando OPDIVO® é administrado em monoterapia, a dose prescrita para o paciente é 240 mg ou 480 mg administrados independentemente do peso corporal.
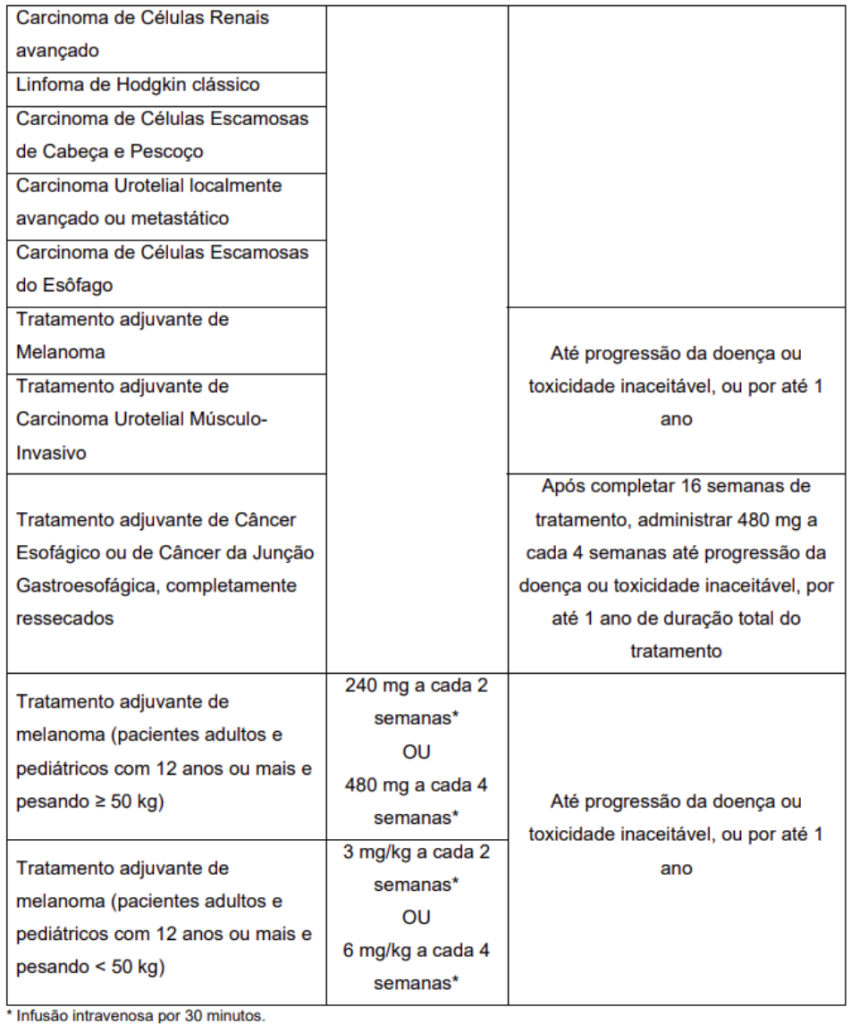
Quando OPDIVO® é administrado em combinação com ipilimumabe para melanoma, CCR ou CHC, as 4 doses iniciais para o paciente são dadas em mg/kg. A dose total em mg = o peso do paciente em kg × a dose prescrita em mg/kg.
Quando OPDIVO® é administrado em combinação com ipilimumabe para MPM, a dose prescrita para o paciente é de 360 mg administrados independentemente do peso corporal.
O volume de OPDIVO® concentrado para preparar a dose (mL) = a dose total em mg, dividida por 10 (a concentração de OPDIVO® é 10 mg/mL).
Ajuste de dose
Insuficiência renal: não há ajustes de dosagem previstos na bula do fabricante.
Insuficiência hepática: não há ajustes de dosagem previstos na bula do fabricante.
Preparo
A preparação deve ser realizada por profissionais treinados de acordo com os procedimentos de boas práticas especialmente com relação à assepsia. OPDIVO® (nivolumabe) pode ser usado para administração intravenosa:
– Sem diluição, após transferência para um recipiente de infusão usando uma seringa estéril apropriada.
– Após diluição:
* No caso de dose fixa (240 mg ou 480 mg): OPDIVO® concentrado pode ser diluído contanto que o volume de infusão total não exceda 160 mL.
* No caso de dose com base no peso (fase combinação): a concentração final da infusão deve estar entre 1 e 10 mg/mL.
– Para pacientes com peso corporal inferior a 40 kg, o volume total de infusão não deve exceder 4 mL/kg de peso corporal.
– O OPDIVO® concentrado pode ser diluído com:
* Solução injetável de cloreto de sódio 9 mg/mL (0,9%); ou
* Solução injetável de glicose 50 mg/mL (5%).
ETAPA 1
Inspecione o OPDIVO® concentrado quanto a materiais particulados ou descoloração. Não agite o frasco. O OPDIVO® concentrado é um líquido límpido a opalescente, incolor a amarelo pálido. Descarte o frasco se a solução estiver turva, descolorida, ou contenha material particulado além de algumas partículas translúcidas a esbranquiçadas.
Retire o volume necessário de OPDIVO® concentrado usando uma seringa estéril apropriada.
ETAPA 2
Transfira o OPDIVO® concentrado para um frasco de vidro estéril vazio ou uma bolsa intravenosa (PVC ou poliolefina).
Se aplicável, dilua com o volume necessário de solução injetável de cloreto de sódio 9 mg/mL (0,9%) ou solução injetável de glicose 50 mg/mL (5%). Para facilitar o preparo, o concentrado pode também ser transferido diretamente para uma bolsa preenchida contendo o volume adequado de solução cloreto de sódio para injeção de 9 mg/mL (0,9%) ou 50 mg/mL (5%) de solução de glicose para injeção.
Vias de administração
INTRAVENOSO
Administração
A infusão de OPDIVO® (nivolumabe) não deve ser administrada como injeção rápida ou por bolus.
Administre a infusão de OPDIVO® (nivolumabe) por via intravenosa durante um período de 30 minutos. Utilize um equipo de infusão e um filtro em linha estéril, não pirogênico de baixa ligação proteica (tamanho dos poros de 0,2 µm a 1,2 µm).
A infusão de OPDIVO® (nivolumabe) não deve ser administrada ao mesmo tempo e no mesmo acesso venoso que outros agentes. Utilize um acesso venoso separado para a infusão.
A infusão de OPDIVO® (nivolumabe) é compatível com:
- Recipientes de PVC
- Recipientes de poliolefina
- Frascos de vidro
- Equipo de infusão de PVC
- Filtros em linha com membranas de polietersulfona com tamanho de poros de 0,2 a 1,2 µm.
Após a administração da dose de nivolumabe, lave o equipo com solução injetável de cloreto de sódio 9 mg/mL (0,9%) ou solução injetável de glicose 50 mg/mL (5%).
Quando administrado em combinação com ipilimumabe ou com ipilimumabe e quimioterapia, nivolumabe deve ser fornecido primeiro, seguido do ipilimumabe e então quimioterapia no mesmo dia. Devem ser usadas bolsas de infusão separadas e filtros para cada infusão.
Quando administrado em combinação com quimioterapia contendo fluoropirimidina e platina, nivolumabe deve ser fornecido primeiro, seguido de quimioterapia contendo fluoropirimidina e platina no mesmo dia. Devem ser usadas bolsas de infusão separadas e filtros para cada infusão.
A administração da infusão de OPDIVO® deve ser concluída dentro de 24 horas da sua preparação. Caso não seja utilizada imediatamente, a solução pode ser armazenada em geladeira (2ºC e 8ºC) por não mais que 24 horas e protegida da luz.
Cuidados específicos e monitoramento
População Pediátrica
A segurança e a eficácia de OPDIVO® (nivolumabe) em crianças com menos de 18 anos de idade não foram estabelecidas, exceto em pacientes pediatricos de 12 anos de idade ou mais com melanoma e em combinação com ipilimumabe no tratamento de câncer colorretal.
Idosos
Nenhuma diferença geral na segurança ou eficácia foi relatada entre pacientes idosos (≥ 65 anos) e mais jovens (< 65 anos). Não é necessário ajuste de dose para pacientes idosos (≥ 65 anos). Os dados relativos em pacientes idosos (≥ 75 anos) com CCECP, melanoma adjuvante e CPCNP, e em pacientes com LHc (≥ 65 anos), são limitados para que se possam tirar conclusões acerca desta população.
Os dados em pacientes idosos (≥ 75 anos) com MPM e CHC mostraram uma taxa superior de reações adversas graves e de taxa de descontinuação devido a reações adversas (MPM: 68% e 35% e CHC: 67% e 35%, respectivamente) em relação a todos os indivíduos que receberam nivolumabe em associação com ipilimumabe (MPM: 54% e 28% e CHC: 53% e 27%, respectivamente). Os dados de pacientes com CRC MSI-H ou dMMR mostraram uma maior incidência de reações adversas de Grau 3 ou 4 (55%) em pacientes com ≥ 65 anos que receberam nivolumabe + ipilimumabe, em comparação com aqueles com < 65 anos que receberam a mesma combinação (42%).
Também foi observada uma maior incidência de reações adversas de Grau 3 ou 4 (55%) em pacientes com ≥ 65 anos ou mais tratados com a combinação nivolumabe + ipilimumabe, em comparação com pacientes da mesma faixa etária que receberam nivolumabe como agente único (41%). A incidência de reações adversas de Grau 3 ou 4 foi semelhante entre pacientes com 65 anos ou mais (41%) e aqueles com menos de 65 anos (45%) que receberam nivolumabe como agente único. Pacientes com 65 anos ou mais que receberam nivolumabe com ipilimumabe descontinuaram o tratamento devido a reações adversas em uma taxa maior (23%) em comparação com pacientes da mesma faixa etária que receberam apenas nivolumabe (15%).
Interações medicamentosas
OPDIVO® (nivolumabe) é um anticorpo monoclonal humano; assim sendo, não foram conduzidos estudos de interação farmacocinética. Uma vez que anticorpos monoclonais não são metabolizados pelas enzimas do citocromo P450 (CYP) ou outras enzimas metabolizadoras de medicamentos, não é antecipado que a inibição ou indução dessas enzimas por produtos medicinais co-administrados afete a farmacocinética de OPDIVO®.
Estabilidade/ Conservação
OPDIVO® (nivolumabe) deve ser armazenado em geladeira (2ºC e 8ºC). Não congelar. Não agitar. Manter na embalagem original até o final do uso para proteger da luz. Uma vez aberto, o medicamento deve ser preparado para infusão imediatamente.
Reações adversas
OPDIVO® (nivolumabe) ou OPDIVO® (nivolumabe) em combinação com ipilimumabe ou outros agentes terapêuticos está associado a reações adversas resultantes de atividade imunológica elevada ou excessiva. A maioria delas, incluindo reações graves, foi resolvida após o início da terapia clínica apropriada ou da retirada de nivolumabe.
As reações são apresentadas por classe de sistema orgânico e por frequência. As frequências são definidas como: muito comum (≥ 1/10); comum (≥ 1/100 a < 1/10); incomum (≥ 1/1.000 a < 1/100); rara (≥ 1/10.000 a < 1/1.000); muito rara (< 1/10.000); desconhecido (não é possível estimar a frequência com dados disponíveis de pós-comercialização). Dentro de cada grupo de frequência, as reações adversas são apresentadas por ordem decrescente de gravidade.
Nivolumabe em monoterapia
As reações adversas relatadas no conjunto de dados agrupado para pacientes tratados com nivolumabe em monoterapia (n=5018) estão apresentados a seguir.
Reações adversas com nivolumabe em monoterapia:
Infecções e infestações: Muito comum: infecção do trato respiratório superior; Comum: pneumoniaa, bronquite
Neoplasmas benignos, malignos e inespecíficos (incluindo cistos e pólipos): Rara: linfadenite histiocítica necrosante (linfadenite de Kikuchi)
Distúrbios do sistema linfático e do sangue: Incomum: eosinofilia
Distúrbios do sistema imunológico: Comum: reação relacionada à infusão, hipersensibilidade (incluindo reação anafilática); Incomum: sarcoidose
Distúrbios endócrinos: Comum: hipotireoidismo, hipertireoidismo; Incomum: insuficiência adrenalb, hipopituitarismo, hipofisite, diabetes mellitus, cetoacidose diabética, tireoidite
Distúrbios de metabolismo e de nutrição: Muito comum: diminuição do apetite; Comum: desidratação; Incomum: acidose metabólica
Distúrbios do sistema nervoso: Muito comum: cefaleia; Comum: neuropatia periférica, tontura; Incomum: polineuropatia, neuropatia autoimune (incluindo paralisia do nervo abducente e facial); Rara: síndrome de Guillain-Barré, desmielinização, síndrome miastênica, encefalitea,c
Distúrbios oculares: Comum: visão embaçada, olho seco; Incomum: uveíte
Distúrbios cardíacos: Comum: taquicardia; Incomum: arritmia (incluindo arritmia ventricular), fibrilação atrial, distúrbios de pericárdiod, miocarditea,e
Distúrbios vasculares: Comum: hipertensão; Incomum: vasculite
Distúrbios respiratórios, torácicos e mediastinais: Muito comum: dispneiaa, tosse; Comum: pneumonitea, derrame pleural; Incomum: infiltração pulmonar
Distúrbios gastrintestinais: Muito comum: diarreia, náusea, constipação, dor abdominal, vômito; Comum: colitea, estomatite, boca seca; Incomum: pancreatite, gastrite; Rara: úlcera duodenal
Distúrbios hepatobiliares: Incomum: hepatite; Rara: colestase
Distúrbios da pele e do tecido subcutâneo: Muito comum: erupção cutâneaf , prurido; Comum: vitiligo, pele seca, eritema, alopecia; Incomum: eritema multiforme, psoríase, rosácea, urticária; Rara: necrólise epidérmica tóxicaa,e, Síndrome de Stevens-Johnsona
Distúrbios musculoesqueléticos e do tecido conjuntivo: Muito comum: dor musculoesqueléticag, artralgia; Comum: artrite; Incomum: polimialgia reumática, miosite (incluindo polimiosite) a; Rara: miopatia, rabdomiólisea,e, síndrome de Sjogren
Distúrbios renais e urinários: Comum: insuficiência renal (incluindo dano renal agudo) a. Rara: nefrite túbulo-intersticial
Distúrbios gerais e condições do local de administração: Muito comum: fadiga, pirexia; Comum: dor, dor torácica, edema (incluindo edema periférico)
Investigações: Comum: redução de peso
a Casos fatais foram reportados em estudos clínicos completos ou em andamento. b Inclui insuficiência adrenal, insuficiência adrenocortical aguda e insuficiência adrenocortical secundária. c Inclui encefalite e encefalite límbica. d Distúrbios pericárdicos é um termo composto que inclui pericardite, derrame pericárdico, tamponamento cardíaco e síndrome de Dressler. e Relatado também em estudos fora do conjunto de dados agrupados. A frequência é fundamentada na exposição em todo o programa. f Erupção cutânea é um termo composto, que inclui erupção maculopapular, erupção eritematosa, erupção prurítica, erupção folicular, erupção macular, erupção morbiliforme, erupção papular, erupção pustular, erupção papuloescamosa, erupção vesicular, erupção generalizada, erupção esfoliativa, dermatite, dermatite acneiforme, dermatite alérgica, dermatite atópica, dermatite bolhosa, dermatite esfoliativa, dermatite psoriasiforme, erupção medicamentosa e penfigoide. g Dor musculoesquelética é um termo composto que inclui dor nas costas, dor nos ossos, dor torácica musculoesquelética, desconforto musculoesquelético, mialgia, dor no pescoço, dor nas extremidades, dor vertebral.
O perfil de segurança global de nivolumabe 3 mg/kg em pacientes com carcinoma hepatocelular previamente tratados com sorafenibe (n=145) foi consistente com o perfil estabelecido em diferentes tipos de tumores para monoterapia com nivolumabe, com exceção de uma incidência maior de níveis de transaminases e bilirrubina elevados.
O perfil de segurança geral do nivolumabe 3 mg/kg em pacientes com carcinoma urotelial avançado ou metastático (n=343) foi consistente com o perfil estabelecido para nivolumabe em monoterapia para os diferentes tipos de tumores.
O perfil de segurança global de nivolumabe a 3 mg/kg para o tratamento de melanoma adjuvante (n=452) foi consistente com o estabelecido em diferentes tipos de tumores para monoterapia com nivolumabe.
Nivolumabe em combinação com ipilimumabe
Resumo tabulado das reações adversas
As reações adversas relatadas no conjunto de dados agrupado para pacientes tratados com nivolumabe em combinação com ipilimumabe (n=448 para melanoma; n=547 para CCR; n=49 para CHC previamente tratado; n=332 para CHC irressecável e n=622 para MPM e CCEE, n=119 para CRC metastático a partir da segunda linha de tratamento e n=200 para CRC metastático em primeira linha) são apresentadas na Tabela 5 e na lista a seguir.
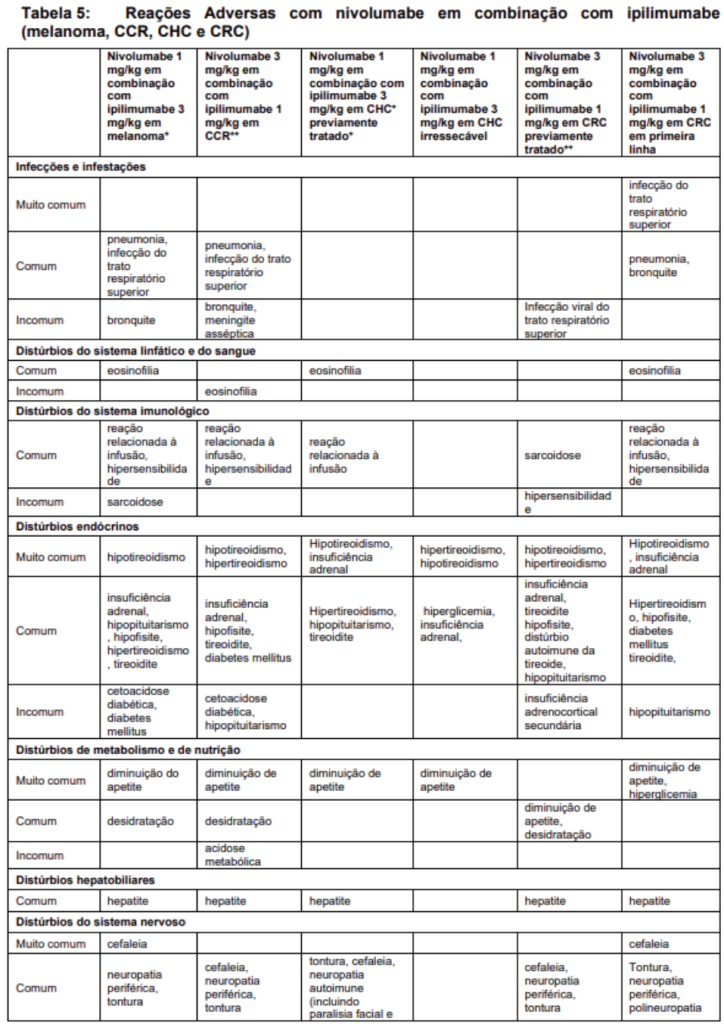
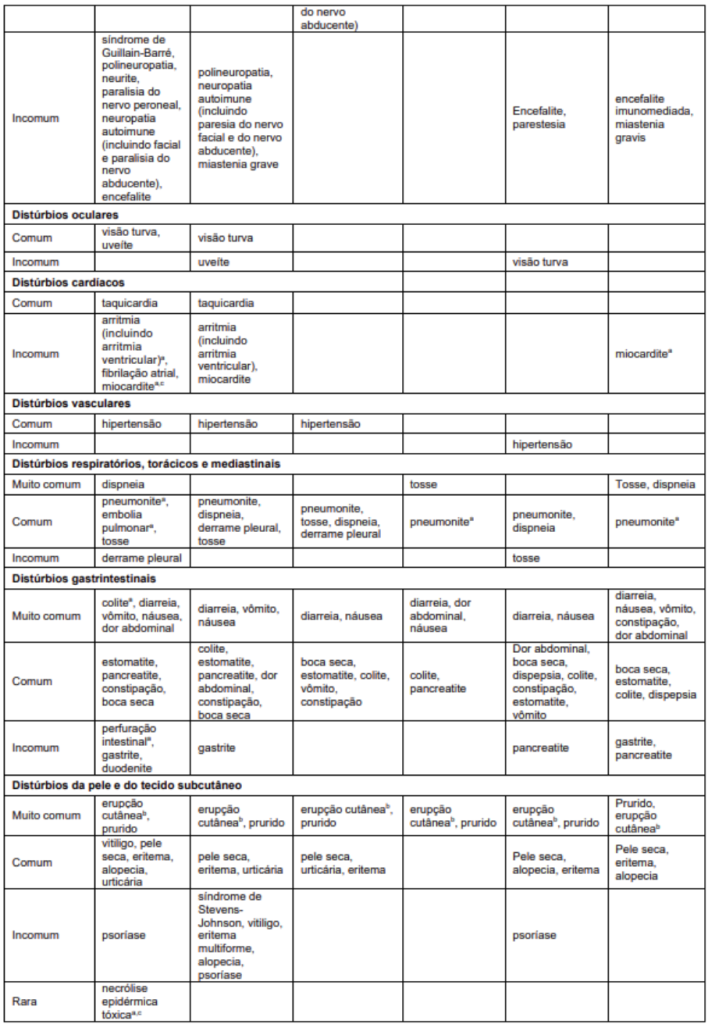
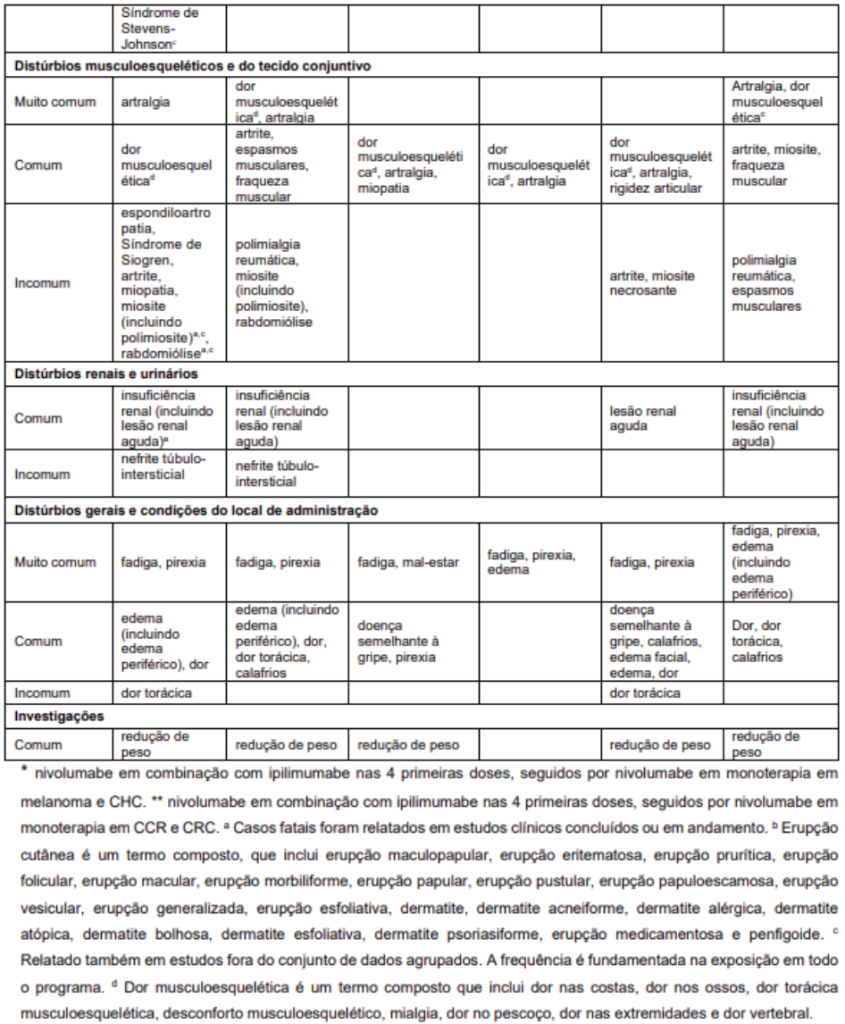
Reações adversas com nivolumabe 3 mg/kg em combinação com ipilimumabe 1 mg/kg (MPM e CCEE):
Infecções e infestações: Muito comum: pneumonia; Comum: infecção do trato respiratório superior
Distúrbios do sistema imunológico: Comum: reação relacionada à infusão, hipersensibilidade
Distúrbios endócrinos: Muito comum: hipotireoidismo; Comum: hipertireoidismo, insuficiência adrenal, hipofisite, hipopituitarismo, diabetes mellitus, tireoidite
Distúrbios de metabolismo e de nutrição: Muito comum: diminuição do apetite
Distúrbios hepatobiliares: Comum: hepatite Distúrbios do sistema nervoso: Incomum: encefalite
Distúrbios oculares: Incomum: uveíte
Distúrbios cardíacos: Incomum: miocardite
Distúrbios respiratórios, torácicos e mediastinais: Comum: pneumonitea
Distúrbios gastrintestinais: Muito comum: diarreia, náusea, constipação; Comum: colite, pancreatite
Distúrbios da pele e do tecido subcutâneo: Muito comum: erupção cutâneab, prurido
Distúrbios musculoesqueléticos e do tecido conjuntivo: Muito comum: dor musculoesqueléticac, Comum: artrite; Incomum: miosite
Distúrbios renais e urinários: Comum: insuficiência renal (incluindo lesão renal aguda)
Distúrbios gerais e condições do local de administração: Muito comum: fadiga, pirexia
a Casos fatais foram relatados em estudos clínicos concluídos ou em andamento. b Erupção cutânea é um termo composto, que inclui erupção maculopapular, erupção eritematosa, erupção prurítica, erupção folicular, erupção macular, erupção morbiliforme, erupção papular, erupção pustular, erupção papuloescamosa, erupção vesicular, erupção generalizada, erupção esfoliativa, dermatite, dermatite acneiforme, dermatite alérgica, dermatite atópica, dermatite bolhosa, dermatite esfoliativa, dermatite psoriasiforme, erupção medicamentosa e penfigoide. c Dor musculoesquelética é um termo composto que inclui dor nas costas, dor nos ossos, dor torácica musculoesquelética, desconforto musculoesquelético, mialgia, dor no pescoço, dor nas extremidades e dor vertebral.
Nivolumabe em combinação com ipilimumabe e quimioterapia
CPCNP
Resumo de reações adversas
As reações adversas relatadas no conjunto de dados para pacientes tratados com nivolumabe 360 mg em combinação com ipilimumabe 1 mg/kg e 2 ciclos de quimioterapia à base de platina (n=358) são apresentadas a seguir.
Reações adversas com nivolumabe em combinação com ipilimumabe e quimioterapia*:
Infecções e infestações: Comum: conjuntivite, pneumonia, infecção do trato respiratório
Distúrbios do sangue e do sistema linfático: Comum: neutropenia febril; Incomum: eosinofilia
Distúrbios do sistema imunológico: Comum: reação relacionada à infusão, hipersensibilidade
Distúrbios endócrinos: Muito comum: hipotireoidismo; Comum: hipertireoidismo, insuficiência adrenal, hipofisite, tireoidite; Incomum: hipopituitarismo, hipoparatireoidismo
Distúrbios metabólicos e da nutrição: Muito comum: diminuição do apetite; Comum: desidratação, hipoalbunemia, hipofosfatemia
Distúrbios do sistema nervoso: Comum: neuropatia periférica, tontura; Incomum: polineuropatia, neuropatia autoimune (incluindo paresia facial e do nervo abducente), encefalite
Distúrbios oculares: Comum: olho seco; Incomum: visão turva, episclerite
Distúrbios cardíacos: Incomum: taquicardia, fibrilação atrial, bradicardia
Distúrbios vasculares: Incomum: hipertensão
Distúrbios respiratórios, torácicos e do mediastino: Comum: pneumonite, dispneia, tosse; Incomum: derrame pleural
Distúrbios gastrointestinais: Muito comum: náusea, diarreia, vômito; Comum: constipação, estomatite, dor abdominal, colite, boca seca, pancreatite
Distúrbios hepatobiliares: Comum: hepatite
Distúrbios de pele e do tecido subcutâneo: Muito comum: erupção cutâneaa, prurido; Comum: alopecia, pele seca, eritema, urticária; Incomum: psoríase, síndrome de Stevens-Johnson, vitiligo
Distúrbios musculoesqueléticos e de tecido conjuntivo: Comum: dor musculoesqueléticab, artralgia, artrite; Incomum: fraqueza muscular, espasmos musculares, polimialgia reumática
Distúrbios renais e urinários: Comum: insuficiência renal (incluindo lesão renal aguda); Incomum: nefrite
Distúrbios gerais e condições do local de administração: Muito comum: fadiga; Comum: pirexia, edema (incluindo edema periférico); Incomum: calafrios, dor torácica
Investigações: Comum: aumento do hormônio tireoestimulante; Incomum: aumento de gamaglutamiltransferase
* Nivolumabe a cada 3 semanas em combinação com ipilimumabe a cada 6 semanas e quimioterapia à base de platina a cada 2 ciclos, então seguidos por nivolumabe a cada 3 semanas em combinação com ipilimumabe a cada 6 semanas no CPCNP. a Erupção cutânea é um termo composto que inclui erupção maculopapular, erupção eritematosa, erupção pruriginosa, erupção macular, erupção morbiliforme, erupção papular, erupção generalizada, dermatite, dermatite acneiforme, dermatite alérgica, dermatite atópica, dermatite bolhosa e erupção medicamentosa. b Dor musculoesquelética é um termo composto que inclui dor nas costas, dor óssea, dor musculoesquelética torácica, mialgia, dor cervical, dor em extremidade e dor vertebral.
Nivolumabe em combinação com quimioterapia
Resumo tabulado das reações adversas
As reações adversas relatadas no conjunto de dados para pacientes tratados com nivolumabe 360 mg em combinação com quimioterapia dupla à base de platina em CPCNP ressecável em tratamento neoadjuvante (n=176), nivolumabe 360 mg em combinação com quimioterapia dupla à base de platina, seguido por nivolumabe 480 mg após cirurgia em CPCNP ressecável (n = 228), e nivolumabe 240 mg ou 360 mg em combinação com quimioterapia em CG, CJEG e ACE (n = 782), assim como as reações relatadas para pacientes tratados com nivolumabe 240 mg a cada 2 semanas em combinação com quimioterapia em primeira linha de CCEE (n=310) e pacientes tratados com nivolumabe 360 mg em combinação com quimioterapia no tratamento de CU (n=304), são apresentadas na Tabela 6.
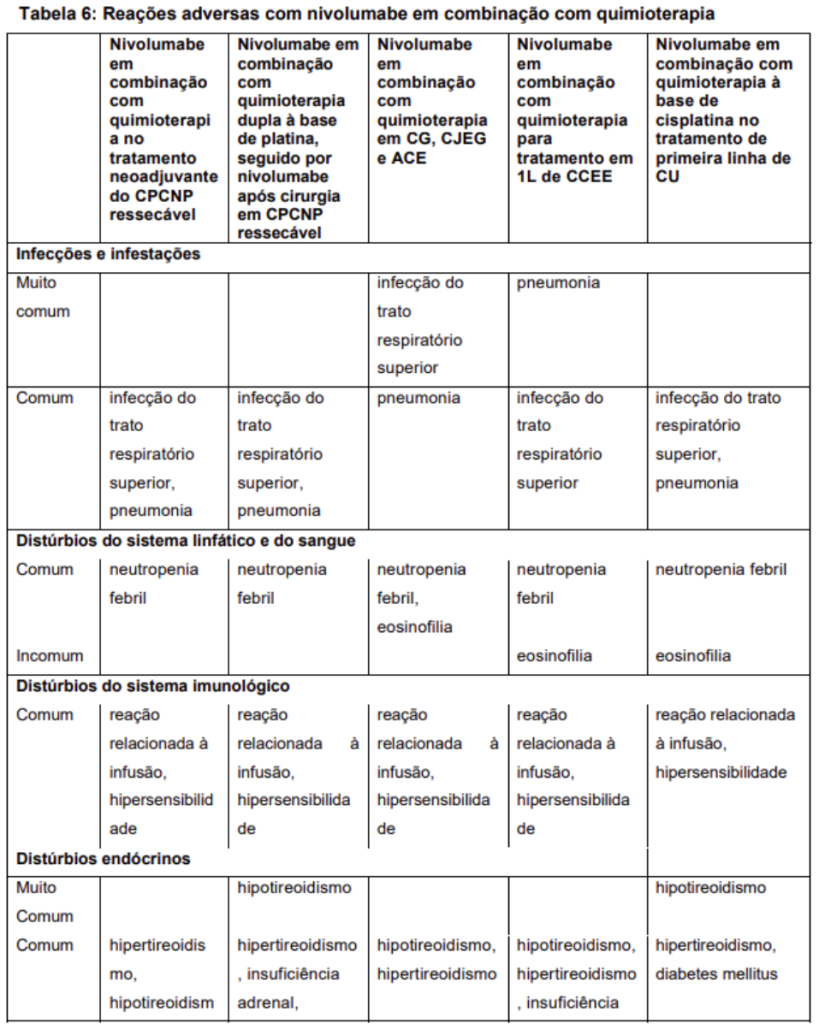
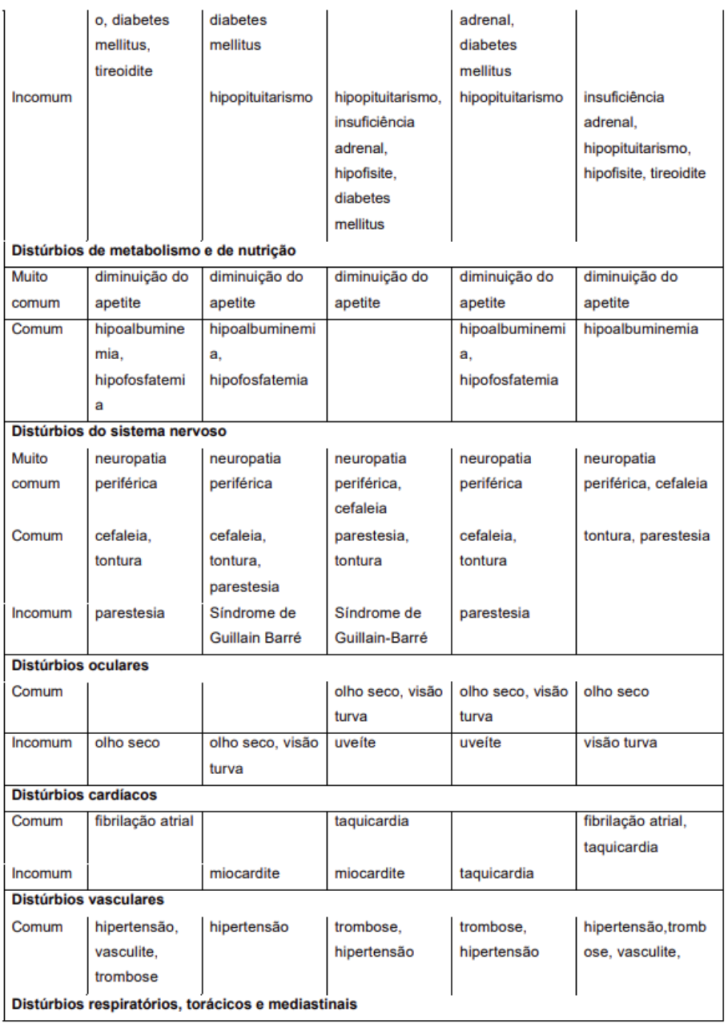
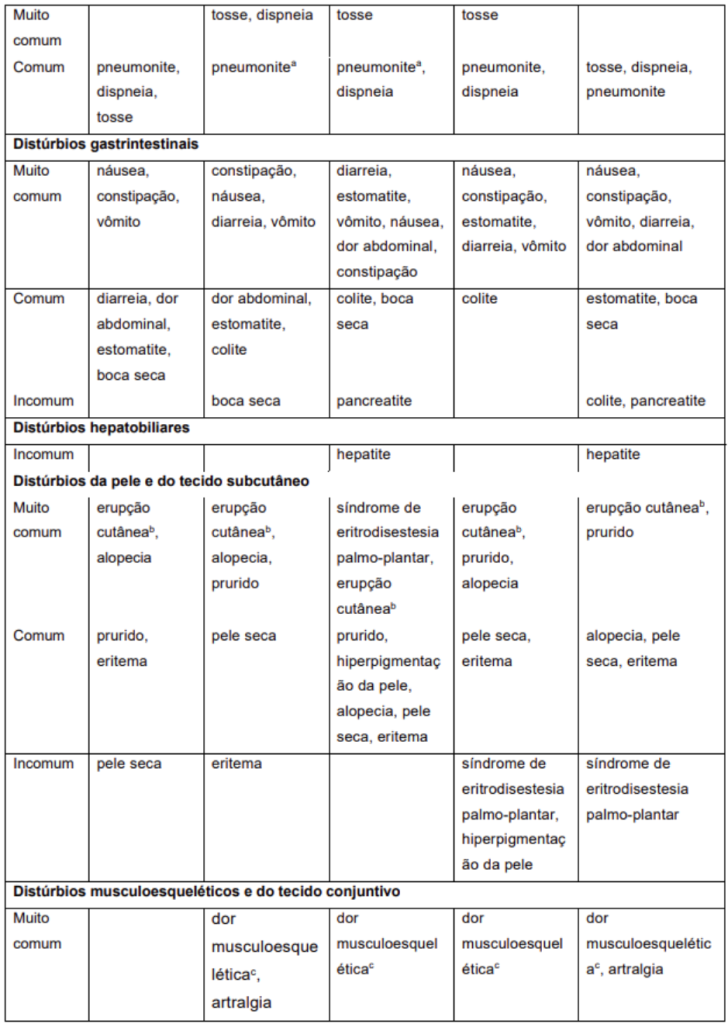
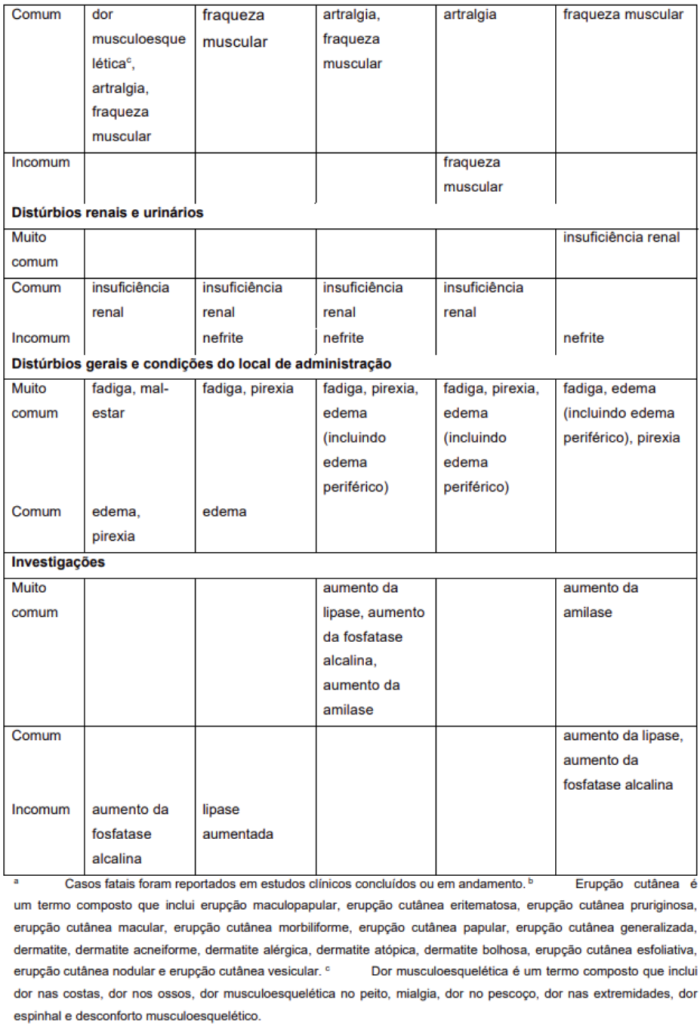
Nivolumabe em combinação com cabozantinibe
Quando nivolumabe for administrado em combinação com cabozantinibe, consulte as informações na bula de cabozantinibe antes do início do tratamento. Para informações adicionais sobre o perfil de segurança de cabozantinibe em monoterapia, consulte as Informações na bula de cabozantinibe.
Resumo de reações adversas
Reações adversas relatadas no conjunto de dados para pacientes tratados com nivolumabe 240 mg em combinação com cabozantinibe 40 mg (n = 320) são apresentados a seguir.
Reações adversas com nivolumabe em combinação com cabozantinibe:
Infecções e infestações: Muito comum: infecção do trato respiratório superior; Comum: pneumonia
Distúrbios do sangue e sistema linfático: Comum: eosinofilia
Distúrbios do sistema imunológico: Comum: hipersensibilidade (incluindo reação anafilática); Incomum: reação de hipersensibilidade relacionada à infusão
Distúrbios endócrinos: Muito comum: hipotireoidismo, hipertireoidismo; Comum: insuficiência adrenal; Incomum: hipofisite, tireoidite
Distúrbios do metabolismo e nutrição: Muito comum: diminuição do apetite; Comum: desidratação Distúrbios do sistema nervoso: Muito comum: disgeusia, cefaleia, tontura; Comum: neuropatia periférica; Incomum: encefalite autoimune, síndrome de Guillain-Barré, síndrome miastênica
Distúrbios do ouvido e labirinto: Comum: tinido
Distúrbios oculares: Comum: olho seco, visão turva; Incomum: uveíte
Distúrbios cardíacos: Comum: fibrilação atrial, taquicardia; Incomum: miocardite
Distúrbios vasculares: Muito comum: hipertensão; Comum: trombosea
Distúrbios respiratórios, torácicos e mediastinais: Muito comum: dispneia, tosse, disfonia; Comum: pneumonite, embolia pulmonar, derrame pleural, epistaxe
Distúrbios gastrointestinais: Muito comum: diarreia, vômito, náusea, constipação, estomatite, dor abdominal, dispepsia; Comum: colite, gastrite, dor oral, boca seca, hemorroidas; Incomum: pancreatite, perfuração no intestino delgadob, glossodínia
Distúrbios hepatobiliares: Comum: hepatite
Distúrbios da pele e tecido subcutâneo: Muito comum: síndrome de eritrodisestesia palmoplantar, erupção cutâneac, prurido; Comum: pele seca, alopecia, eritema, alteração na cor do cabelo; Incomum: psoríase, urticária
Distúrbios musculoesqueléticos e do tecido conjuntivo: Muito comum: dor musculoesqueléticad, artralgia, espasmo muscular; Comum: artrite; Incomum: miopatia, osteonecrose da mandíbula, fístula
Distúrbios renais e urinários: Muito comum: proteinúria; Comum: insuficiência renal, lesão renal aguda; Incomum: nefrite
Distúrbios gerais e condições no local da administração: Muito comum: fadiga, pirexia, edema; Comum: dor, dor torácica
Investigações: Muito comum: redução de peso
a Trombose é um termo composto que inclui trombose da veia porta, trombose da veia pulmonar, trombose pulmonar, trombose aórtica, trombose arterial, trombose venosa profunda, trombose da veia pélvica, trombose da veia cava, trombose venosa, trombose venosa no membro. b Casos fatais foram relatados. c Erupção cutânea é um termo composto que inclui dermatite, dermatite acneiforme, dermatite alérgica, dermatite atópica, dermatite bolhosa, erupção cutânea esfoliativa, erupção eritematosa, erupção cutânea folicular, erupção macular, erupção maculopapular, erupção papular, erupção morbiliforme, erupção cutânea pruriginosa e erupção cutânea erupção. d Dor musculoesquelética é um termo composto que inclui dor nas costas, dor óssea, dor torácica musculoesquelética, desconforto musculoesquelético, mialgia, dor no pescoço, dor nas extremidades, dor na coluna.
Contraindicações
Hipersensibilidade à substância ativa ou a quaisquer excipientes.
Fonte:
Opdivo®. [Bula]. São Paulo: Bristol-Myers Squibb Farmacêutica LTDA. Disponível em: https://consultas.anvisa.gov.br/#/bulario/q/?numeroRegistro=101800408: 18/08/2025
