Nome Comercial/ Apresentação
ENHERTU® (trastuzumabe deruxtecana) 100mg/ Pò liofilizado para solução injetável
Classe Terapêutica
Antineoplásico, Anticorpo monoclonal
Indicação
- Câncer de mama HER2-positivo;
- Câncer de mama HER2 baixo ou ultrabaixo;
- Câncer de pulmão de não pequenas células (CPNPC);
- Câncer gástrico / junção gastroesofágica HER2-positivo;
- Outros tumores sólidos HER2-positivos.
Dose
Câncer de mama, irressecável ou metastásico, HER2-positivo
Uso a cada três semanas: IV- 5,4 mg/kg uma vez a cada 3 semanas até progressão da doença ou toxicidade inaceitável.
Câncer colorretal, metastásico, expressando HER2 (off-label)
Uso a cada três semanas: IV- 6,4 mg/kg uma vez a cada 3 semanas até progressão da doença ou toxicidade inaceitável.
Câncer gástrico, localmente avançado ou metastásico, HER2-positivo
Uso a cada três semanas: IV- 6,4 mg/kg uma vez a cada 3 semanas até progressão da doença ou toxicidade inaceitável. Selecione os pacientes para terapia com base na superexpressão da proteína HER2 ou na amplificação do gene HER2. Se possível obter uma nova amostra de tumor, reavaliar o status de HER2 entre a terapia anterior com trastuzumabe e fam-trastuzumabe deruxtecano.
Câncer de pulmão de células não pequenas, metastático, recidivante/refratário, não escamoso, mutante HER2 (uso off-label):
Uso a cada três semanas: IV- 6,4 mg/kg uma vez a cada 3 semanas até progressão da doença ou toxicidade inaceitável.
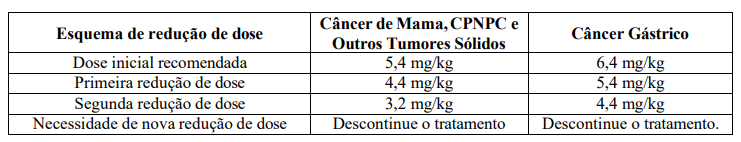
Ajuste de dose
Redução de dose por toxicidade: A dose inicial é de 5,4 mg/kg, se houver necessidade a primeira redução da dose é para 4,4 mg/kg, seguida de 3,2 mg/kg
Insuficiência renal: Não é necessário ajuste de dose em pacientes com insuficiência renal leve ou moderada. Não existem dados disponíveis para pacientes com insuficiência renal grave.
Insuficiência hepática: Não é necessário ajuste de dose em pacientes com insuficiência hepática leve. Os dados disponíveis são insuficientes para realizar qualquer recomendação de ajuste de dose para pacientes com insuficiência hepática moderada.
Preparo
Reconstituição
- Preparar imediatamente antes da diluição
- Pode ser necessário mais de um frasco para a dose total
- Adicionar 5 mL de água estéril em cada frasco-ampola de 100 mg
- Obter concentração final de 20 mg/mL
- Misturar suavemente (movimentos circulares) — não agitar
-
Solução reconstituída:
- Refrigerada (2–8°C) até 24h
- Proteger da luz
- Não congelar
- Sem conservantes → descartar após 24h se não utilizada
Diluição
- Calcular volume necessário
- Retirar volume calculado da solução reconstituída
- Diluir em 100 mL de glicose 5% (não usar NaCl)
- Bolsa recomendada: PVC ou poliolefina
- Misturar suavemente (não agitar)
- Proteger da luz
Vias de administração
INTRAVENOSO
Administração
Administre ENHERTU® como infusão intravenosa usando apenas conjunto de infusão de poliolefina ou polibutadieno e filtro em linha de polietersulfona (PES) ou polisulfona (PS) de 0,20 ou 0,22 micron. Não administre por injeção intravenosa direta ou em bolus. Cubra a bolsa de infusão para proteger a solução da luz.
Cuidados específicos e monitoramento
Doença pulmonar intersticial (DPI) / pneumonite
- Pode ser grave ou fatal
- Monitorar sintomas respiratórios (tosse, dispneia, febre)
- Grau 1: considerar corticosteroide e suspender temporariamente
- Grau ≥2: tratar com corticosteroide e descontinuar definitivamente
- Incidência até ~15%, com casos fatais raros
Neutropenia
- Frequente e potencialmente grave (inclui neutropenia febril)
- Exige hemograma regular
- Pode requerer redução ou interrupção da dose
- Incidência de grau 3–4 até ~28% e neutropenia febril ~1–2,6%
Disfunção ventricular esquerda
- Redução da FEVE pode ocorrer
- Monitorização cardíaca necessária
- Suspender se FEVE <40% ou queda >20% da basal
- Descontinuar em insuficiência cardíaca sintomática
Gravidez e lactação
- Contraindicado na gravidez (risco de toxicidade fetal grave)
- Contracepção obrigatória: mulheres (7 meses) e homens (4 meses) após tratamento
- Suspender amamentação durante e até 7 meses após tratamento
Interações medicamentosas
Efeitos de outros medicamentos na farmacocinética de ENHERTU® Estudos in vitro indicam que o inibidor da topoisomerase I é metabolizado principalmente pela CYP3A4 e é substrato dos seguintes transportadores: glicoproteína-P (P-gp), OATP1B1, OATP1B3, MATE2-K, MRP1 e BCRP.
A coadministração com ritonavir (200 mg 2x/dia do dia 17 do ciclo 2 ao dia 21 do ciclo 3), inibidor duplo de OATP1B/CYP3A, aumentou a exposição (ASC) do trastuzumabe deruxtecana em 19% e do inibidor da topoisomerase I livre em 22%.
A coadministração com itraconazol (200 mg 2x/dia do dia 17 do ciclo 2 ao dia 21 do ciclo 3), inibidor potente da CYP3A, aumentou a exposição (ASC) do trastuzumabe deruxtecana em 11% e do inibidor da topoisomerase I livre em 18%. Não se espera que o impacto dessas alterações seja clinicamente significativo.
Não é necessário ajuste de dose durante a administração concomitante de ENHERTU® com medicamentos inibidores da OATP1B ou CYP3A. Não é esperada interação clinicamente significativa com medicamentos inibidores da P-gp, MATE2-K. MRP1 ou transportadores BCRP.
Reações adversas
Sistema/efeito | Reações principais | Importância clínica |
|---|---|---|
Gastrointestinal | Náusea, vômito, diarreia, constipação, dor abdominal | Muito frequentes, geralmente manejáveis |
Hematológico | Neutropenia, anemia, leucopenia, trombocitopenia | Pode ser grave, requer monitorização |
Respiratório | Doença pulmonar intersticial (DPI), dispneia, tosse | Evento crítico, pode ser fatal |
Geral | Fadiga, astenia, dor musculoesquelética | Frequente |
Hepático | ↑ transaminases, bilirrubina | Monitorização obrigatória |
Cardíaco | Redução da fração de ejeção do VE | Pode exigir suspensão do tratamento |
Outros | Alopecia, hipocalemia, perda de peso, reações à infusão | Frequentes |
Contraindicações
ENHERTU® é contraindicado para pacientes com hipersensibilidade ao trastuzumabe deruxtecana ou a qualquer dos componentes da formulação.
Fonte:
ENHERTU. Bula do profissional de saúde. São Paulo: Daiichi Sankyo Brasil Farmacêutica Ltda., 2025. Disponível em: https://daiichisankyo.com.br/wp-content/uploads/2025/09/bula-enhertu-profissional-db06_29.09.pdf. Acesso em: 16 abr. 2026.
.
