Nome Comercial/ Apresentação
SARCLISA (isatuximabe) 20 mg/mL concentrado para solução para perfusão. Frascos com 100 mg de isatuximab em 5 mL de concentrado (100 mg/5 mL) e com 500 mg de isatuximab em 25 mL de concentrado (500 mg/25 mL).
Classe Terapêutica
Anticorpo citolítico direcionado ao CD-38.
Indicação
Indicado, em combinação com pomalidomida e dexametasona, para o tratamento de doentes adultos com mieloma múltiplo (MM) em recidiva e refratário que receberam pelo menos duas terapêuticas anteriores, incluindo lenalidomida e um inibidor do proteosoma (IP) e que demonstraram progressão de doença na última terapêutica.
Dose
A dose recomendada de SARCLISA é de 10 mg/kg de peso corporal, administrado como perfusão intravenosa em combinação com pomalidomida e dexametasona (regime de isatuximab), de acordo com o esquema:

Ajuste de dose:
Insuficiência Renal: Com base na análise farmacocinética da população e segurança clínica, não é recomendado qualquer ajuste posológico em doentes com compromisso renal ligeiro a grave
Insuficiência hepática: Com base na análise farmacocinética da população, não é recomendado qualquer ajuste posológico em doentes com compromisso hepático ligeiro. Os dados em doentes com compromisso hepático moderado a grave são limitados (ver secção 5.2), mas não existe evidência que sugira que é necessário um ajuste da dose nestes doentes.
Vias de administração
VIA INTRAVENOSA
Preparo e administração
Retire a quantidade apropriada (mL) dos frascos de isatuximabe 20 mg/mL para a dose calculada (use o peso corporal real). De uma bolsa de 250 mL para injeção de cloreto de sódio a 0,9% ou dextrose a 5%, retire uma quantidade (mL) de diluente igual à quantidade de medicamento a ser injetado. Injete a dose calculada de isatuximabe na bolsa de infusão. Inverta delicadamente o saco para misturar a solução, mas não agite.
Após a diluição, a perfusão de SARCLISA deve ser administrada por via intravenosa de acordo com a velocidade de perfusão apresentada na tabela abaixo. O aumento incremental da velocidade de perfusão deve ser considerado apenas na ausência de reações à perfusão.
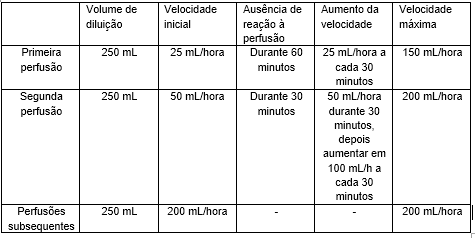
Cuidados e orientações
As mulheres com potencial de engravidar tratadas com isatuximab devem utilizar métodos contraceptivos eficazes durante o tratamento e pelo menos, 5 meses após terminar o tratamento.
Use isatuximabe com cautela em pacientes com infecção. Infecções graves e fatais, incluindo infecções oportunistas, já ocorreram. Use isatuximabe com cautela em pacientes com histórico de herpes zoster; pode ocorrer reativação do vírus varicela-zoster latente.
Interações medicamentosas
O isatuximabe, por ser um medicamento imunossupressor, pode reduzir a eficácia de vacinas, em particular: Vacina contra cólera, Vacina Tetravalente contra Dengue, Vacinas contra SARS-CoV-2 (COVID-19), Vacina de mRNA contra o vírus SARS-CoV-2 (COVID-19), Vacina de nanopartículas de proteína spike recombinante do vírus SARS-CoV-2 (COVID-19). Recomenda-se, sempre que possível, administrar vacinas antes do início do tratamento. Pacientes devem ser orientados a manter medidas de prevenção mesmo após a vacinação, devido à possível resposta imune atenuada.
Estabilidade/ Conservação
Usar dentro de 48 horas quando armazenado refrigerado (2 a 8 graus C ou 36 a 46 graus F), seguido de 8 horas (incluindo o tempo de infusão) em temperatura ambiente.
Reações adversas
As reações adversas mais frequentes (>20%) são neutropenia (46,7%), reações à perfusão (38,2%), pneumonia (30,9%), infeções das vias respiratórias superiores (28,3%), diarreia (25,7%) e bronquite (23,7%). As reações adversas graves mais frequentes são pneumonia (9,9%) e neutropenia febril (6,6%).
Contraindicações:
Hipersensibilidade à substância ativa ou a qualquer um dos excipientes.
Fonte:
SARCLISA ®. [Bula]. São Paulo: Sanofi-Aventis Deutschland GmbH. Disponível em: https://ec.europa.eu/health/documents/communityregister/2020/20200530148173/anx_148173_pt.pdf. Consultado em 25/08/2025.
CLINICALKEY. Isatuximabe – monografia de medicamento. [Internet]. Disponível em: https://www.clinicalkey.com/#!/content/drug_monograph/6-s2.0-5208#Interactions. Acesso em: 26 ago. 2025.
